Prototyp eines medizinischen Geräts Die Kernaufgabe von , die Einhaltung gesetzlicher Vorschriften sicherzustellen, unterscheidet sich grundlegend von allgemeinen technischen Prototypen. Tatsächlich ist dies die Hauptursache für Missverständnisse über langsame Iteration. Im traditionellen Modell wird die funktionale und regulatorische Verifizierung getrennt; Angesichts regulatorischer Herausforderungen wie Biokompatibilität und elektrische Sicherheit müssen daher später drastische Änderungen am Prototyp vorgenommen werden, was die klinischen Studien und die Registrierung erheblich verzögert.
Die „ Registration-Oriented Prototyping “-Strategie von LS Manufacturing integriert die regulatorischen Anforderungen bereits in der Designphase systematisch. Standards stehen ganz oben auf der Prioritätenliste, um sicherzustellen, dass die wichtigsten Registrierungselemente in Verbindung mit der funktionalen Umsetzung des Prototyps erfüllt werden, sodass der Prototyp für die klinische Validierung und Registrierungstests qualifiziert ist und so den ersten Erfolg bei der Produkteinführung gewährleistet. Um Ihnen Zeit zu sparen, finden Sie hier einen kurzen Überblick über die wichtigsten Ergebnisse.
Kurzreferenz zum Prototyping medizinischer Geräte
| Modul | Schlüssel zum Mitnehmen |
| Kernkonzept | Erstellen Sie „ Registrierungsgesteuerte Prototypen “, die Funktion und Einhaltung gesetzlicher Vorschriften vereinen. |
| Traditionelle Schmerzpunkte | Die Einführung regulatorischer Anforderungen zu einem späten Zeitpunkt im Prozess führt zu wiederholten Änderungen am Prototyp, was die Markteinführung verzögert. |
| Schlüsselelemente | Biokompatibilität, Usability Engineering und Risikomanagement sollen in der Prototyping-Phase gemeinsam berücksichtigt werden. |
| Lösung | Machen Sie das Design gleich beim ersten Mal richtig – durch proaktive behördliche Überwachung und durch paralleles Arbeiten. |
| Ultimativer Wert | Das Registrierungsrisiko wird drastisch reduziert und der gesamte Produkteinführungszyklus wird erheblich verkürzt. |
Die folgende Tabelle zeigt, wie die Entwicklung medizinischer Geräte beschleunigt werden kann durch die Verschiebung der regulatorischen Anforderungen Von der „Hürde im Spätstadium“ zum „Entwurfsinput im Frühstadium“. Die Entwicklung hin zu einem „registrierungsorientierten“ Ansatz bedeutet, dass der Prototyp selbst zur Grundlage für die Registrierung wird, ohne dass später störende Änderungen vorgenommen werden müssen, mit dem Ziel einer effizienten, zuverlässigen und schnellen Markteinführung.
Warum diesem Leitfaden vertrauen? Praxiserfahrung von LS-Fertigungsexperten
Es gibt online mehrere tausend Artikel zum Thema Prototyping für medizinische Geräte – warum sollten Sie sich also die Zeit nehmen, diesen Artikel zu lesen? Was wir hier teilen, stammt nicht aus einer Lehrbuchdefinition, sondern vielmehr aus einigen praktischen Richtlinien, die an die strengen Einschränkungen der ISO 13485 gebunden sind ISO9001 System entwickelt und durch unzählige Operationen und Testergebnisse validiert.
Seit über einem Jahrzehnt hat unser Team mehr als 50.000 kundenspezifische Prototypen hergestellt, die den Anforderungen entsprechen ISO 13485 für Medizinprodukte Anforderungen an das Qualitätssystem. Jedes Projekt vermittelte uns ein tieferes Verständnis dafür, wie man die Schnittparameter für biologisch abbaubare Magnesiumlegierungen ohne thermische Beschädigung einstellt, wie man die Stabilität in dünnwandigen Strukturen beim Mikrofräsen aufrechterhält und wie man gleichzeitig die Anforderungen des Risikomanagements und der Usability Engineering in jedem Schritt der Iteration umsetzt.
Vertrauen Sie uns, was Sie hier lesen, ist die Kernmethode, die wir täglich nutzen, um Herausforderungen zu meistern. Lassen Sie uns zusammenarbeiten, um Ihre neuartigen Ideen effizient und zuverlässig in vertrauenswürdige Produkte umzusetzen.

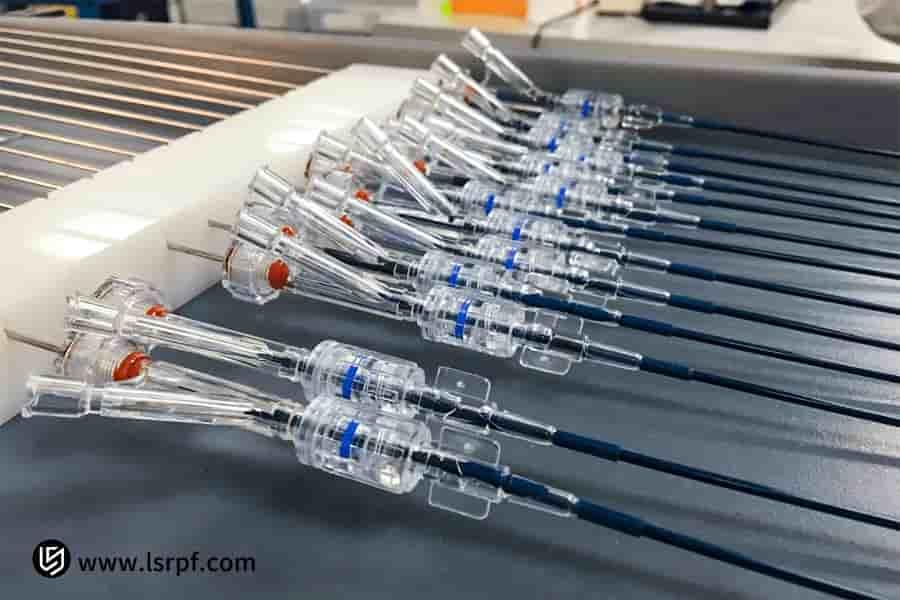
Abbildung 1: Umfangreicher Prototyp zur Funktionsüberprüfung durch LS Manufacturing
Warum sollten Prototypen medizinischer Geräte über die „Funktionsvalidierung“ hinausgehen?
Das ultimative Ziel des Prototyps eines medizinischen Geräts besteht nicht nur darin, ein „funktionierendes“ Modell zu sein, sondern ein „ Produktprototyp “, der alle strengen Registrierungs- und Genehmigungsprozesse bestehen und sicher am menschlichen Körper angewendet werden kann. Daher muss der Umfang der Validierung den gesamten Lebenszyklus der Nutzungsrisiken umfassen.
- Sterilitätstoleranz: Ein Prototyp verfügt möglicherweise über eine einwandfreie motorische Funktion, hält jedoch wiederholten Sterilisationsprozessen wie hohen Temperaturen und Drücken, Bestrahlung oder Eintauchen in Chemikalien möglicherweise nicht stand. Die Alterung des Materials kann seine Leistung verschlechtern und eine klinische Infektion verursachen. In der Prototypenphase müssen konforme Materialien ausgewählt und validiert werden.
- Überblick über die Biokompatibilität: Die Teile, die in direkten oder indirekten Kontakt mit den Patienten kommen , müssen aus ungiftigen und nicht allergischen Materialien bestehen . Dieser Ersatz durch biokompatible Materialien zu einem späteren Zeitpunkt im Designprozess kann sich auf deren mechanische Eigenschaften auswirken und eine vollständige strukturelle Neukonstruktion erforderlich machen.
- Sicherheit und EMV (elektromagnetische Verträglichkeit): Bei aktiven Geräten sollten Prototypen vorab die elektrische Isolierung, den Ableitstrom und andere Sicherheitsindikatoren berücksichtigen, um zu vermeiden, dass während des Betriebs andere Geräte beeinflusst werden, ohne dass sie durch äußere Störungen beeinflusst werden. Eine spätere Nachbesserung wird mit einem astronomisch hohen Preis erkauft, dem bei der Registrierung und Prüfung Rechnung getragen werden muss.
Einbettung der Anforderungen von Einhaltung gesetzlicher Vorschriften Die Entwicklung von Prototypen für medizinische Geräte ist eigentlich ein proaktiver Risikomanagementansatz. Dies würde drastische Designänderungen aufgrund von Funktionsproblemen während der Registrierung und Prüfung oder der klinischen Validierung vermeiden – was im Wesentlichen viel Zeit und Geld spart – und dient als Grundstein für die Beschleunigung der Produkteinführung .
Wie wirkt sich die ISO 13485-Zertifizierung auf das Qualitätssystem für die Prototypenentwicklung aus?
ISO 13485-Prototyp hebt den Prozess von einer potenziell zufälligen Aktivität zu einem kontrollierten, nachvollziehbaren und lebenswichtigen Prozess auf, der frühzeitig Vertrauen in die Sicherheit und Wirksamkeit des Endprodukts schafft. Es erfordert ein robustes Qualitätssystem bereits in der Konzeptphase. Dies spiegelt sich insbesondere wider in:
Strenge Designkontrollen und Dokumentationsmanagement
Für die Prototypenerstellung ist eine Dokumentation der Entwurfseingabe, -ausgabe, -überprüfung und -änderung gemäß der Norm ISO 13485 erforderlich. Es sind vollständig dokumentierte Spezifikationen erforderlich, von Kundenanforderungsspezifikationen über Zeichnungsrevisionsaufzeichnungen bis hin zu Schlussfolgerungen aus der Entwurfsprüfung. Dies sorgt auch für Konsistenz zwischen dem Prototyp und der Designabsicht und bildet eine nützliche „Designhistorie“, die einen direkten Beweis für spätere Registrierungsanträge liefert.
Kontrollierte Herstellung und Rückverfolgbarkeit
Dieser Standard erfordert die Verifizierung und Kontrolle wichtiger Prototyping-Prozesse. Im Hinblick auf die verwendeten medizinischen Materialien sollten beispielsweise Qualifikationszertifikate der Lieferanten und Aufzeichnungen über Eingangskontrollen vorgelegt werden ; Dazu gehört auch die Einrichtung und Bestätigung der Parameter der Bearbeitungsausrüstung, wie z. B. Schichtdicke und Laserleistung 3D-Druck . Dies würde sicherstellen Konsistenz und Wiederholbarkeit in diesem Prototyping-Prozess gewährleisten und eine klare Grundlage für zukünftige Replikation oder Iteration liefern.
Frühzeitige Integration des Risikomanagements
Risikomanagementaktivitäten sollten früh genug während der Prototypenerstellung beginnen, um potenzielle Risiken im Zusammenhang mit Design, Materialien und Prozessen zu identifizieren, für die Kontrollmaßnahmen implementiert werden sollten. In dieser Hinsicht zwingt es das Team , im Voraus über sicherheitsbezogene Anforderungen wie Reinigung und Sterilisation sowie Biokompatibilität nachzudenken , die Lösungen in das Design und die Herstellung des Prototyps zu integrieren und so das Potenzial für größere Designänderungen später zu reduzieren.
Der Wert kommt von a Qualitätssystem während des gesamten Prototyping-Prozesses geht weit über die bloße Erlangung eines Zertifikats nach ISO 13485 hinaus. Dadurch entsteht für den Prototyp selbst ein standardisierter und transparenter Rahmen ; nicht nur ein funktionsfähiges „Muster“, sondern ein zuverlässiges, datenvollständiges und risikokontrolliertes „ Vorprodukt “.
Auswahl medizinischer Materialien, die die Anforderungen an die Biokompatibilität erfüllen?
Die Auswahl ist die erste Hürde bei der Bestimmung der Biokompatibilität und Sicherheit des Produkts bei der Entwicklung des Medizinprodukt-Prototyps . Die Auswahl eines geeigneten Materials minimiert Risiken bei der Registrierung, gewährleistet aber vor allem die Sicherheit des Patienten. Um die Auswahllogik zu verdeutlichen, werden die wichtigsten Überlegungen im Folgenden verglichen.
| Dimensionen der Betrachtung | Grundlegender Pfad: Auswahl zertifizierter Materialien |
Fortgeschrittener Pfad: Biologische Bewertung von Materialien |
| Prinzip | Die Verwendung von medizinische Materialien mit ausgereifter Zertifizierung steht an erster Stelle, wie zum Beispiel USP Class VI oder ISO 10993. | Wenn ein innovatives Material verwendet wird, ist eine vollständige biologische Bewertung gemäß ISO 10993-Standards erforderlich. |
|
Anwendbare Szenarien |
Gilt für die meisten ausgereiften Materialien mit geringem Risiko und einem klaren, schnellen Weg. | Gilt für neue, innovative Materialien oder völlig neue Mensch-Mensch- Interaktionsszenarien mit höherem Risiko und höheren Kosten. |
| Wichtige Beweise | Vollständig ausgefüllte Zertifizierungszertifikate und Prüfberichte des Materiallieferanten. |
Beauftragung eines ordnungsgemäß ausgestatteten und qualifizierten Labors mit der Durchführung aller oder eines Teils der erforderlichen Sicherheitstests. |
| Unsere Unterstützung | Wir bieten schnelle Zuordnungen und Empfehlungen auf der Grundlage einer validierten Datenbank medizinischer Materialien sowie Beratung zu Bewertungsschemata und Testunterstützung. | Wir unterstützen unsere Kunden dabei, Compliance-Risiken entlang des gesamten Prozesses zu mindern. |
Wir empfehlen dringend, die Biokompatibilität bereits in den frühen Phasen des Prototypings zu berücksichtigen und vorzertifizierte Materialien aus validierten Datenbanken auszuwählen, um Unsicherheiten zu minimieren . Wenn der Innovationsbedarf abgedeckt werden soll, muss der gesamte biologische Bewertungspfad lange im Voraus geplant werden. Dies würde Verzögerungen bei der Registrierung und Unterbrechungen der Designs aufgrund von Materialproblemen von Anfang an vermeiden und den Grundstein für die Sicherheit und schnelle Markteinführung von Produkten legen.

Abbildung 2: Präzise volumetrische Steuerung für medizinische Prototypen von LS Manufacturing
Welche Standards sollten Prototypen in verschiedenen klinischen Stadien erfüllen?
Die meisten Menschen interpretieren es falsch Prototyping medizinischer Geräte als eine Aktivität, bei der eine Version eines Prototyps versucht, alle Bedürfnisse zu erfüllen. Dies führt häufig zu einer Verschwendung von Ressourcen bei der Nutzung oder zu fehlenden Standards. Was die Wissenschaft bei jedem Schritt – vom Konzept bis zur klinischen Validierung – genau unterstützt, ist die Erstellung „genau richtiger“ Prototypen, basierend auf den Zielen verschiedener klinischer Phasen.
| Klinisches Stadium | Prototypische Kernziele | Produktionsstandards und -strategien |
| Proof of Concept | Überprüfen Sie so schnell wie möglich die Machbarkeit des Designkonzepts. | Mit wirtschaftlichen und schnellen Methoden wie dem 3D-Druck können Kernfunktionen erreicht werden. Materialien sind grenzenlos; Jetzt ist die Zeit für eine schnelle Iteration. |
| Funktionstests |
Führen Sie umfassende technische Tests von Prototypen durch. |
Gründliche Validierung der Produktleistung und -zuverlässigkeit anhand von Prototypen, die die Produktgröße, Materialien und Leistung genau widerspiegeln. |
| Tierversuche | Der erste Schritt des Verfahrens besteht in der Beurteilung der Sicherheit des jeweiligen Produkts und seiner Biokompatibilität . | Damit die Tests gültig sind, muss es nach aseptischer Verarbeitung aus biokompatiblem medizinischem Material hergestellt werden. |
| Klinische Validierung | Daten zur Sicherheit und Wirksamkeit sollten in Versuchen am Menschen gewonnen werden. | Der Prototyp muss repräsentativ für das Endprodukt sein und diesem entsprechen Normen für Medizinprodukte in Bezug auf Leistung, Materialien und Herstellungsverfahren. |
Im Allgemeinen funktioniert das Prototyping medizinischer Geräte effektiv mit einem dynamischen, aber fortschrittlichen Ansatz. Von der „wirtschaftlichen“ Proof-of-Concept-Phase bis zur „Quasi-Kommerzialisierungsphase“ mit klinische Validierung In jeder Phase des Prototypenentwurfs sollten bestimmte Ziele mit entsprechenden Standards festgelegt werden. Eine solche Strategie wird die F&E-Kosten im Frühstadium effektiv unter Kontrolle halten und gleichzeitig sicherstellen, dass die Integrität und Zuverlässigkeit der Prototypen- Datenkette gewährleistet ist, wodurch Projektverzögerungen oder -ausfälle aufgrund nicht übereinstimmender Prototypenstandards vermieden werden.
Wie können Präzision und Herstellbarkeit beim Prototyp chirurgischer Instrumente in Einklang gebracht werden?
Im Prozess von Prototyp chirurgischer Instrumente Bei der Entwicklung geht es nicht nur darum, eine bessere funktionale Präzision zu erreichen, sondern auch zu beweisen, dass das Design stabil und wirtschaftlich in qualifizierte Massenprodukte umgesetzt werden kann. Den Grundsätzen des Designs für die Herstellbarkeit sollte vorrangige Aufmerksamkeit geschenkt werden. Daher müssen folgende Punkte berücksichtigt werden:
Strukturelle Vereinfachung und Montageoptimierung
Bei gleichzeitiger Gewährleistung der Funktionalität soll die Anzahl der Teile minimiert und aufwändige Innenstrukturen vermieden werden. Beispielsweise könnte integrierte 3D-Drucktechnologie anstelle herkömmlicher mehrteiliger Montagestrukturen eingesetzt werden oder selbstsichernde Schnappkonstruktionen anstelle von Schraubbefestigungen übernommen werden. Dadurch können spätere Montageschwierigkeiten und -zeiten erheblich reduziert und somit die Produktionseffizienz und -konsistenz verbessert werden.
Passende Fertigungsprozesse und tolerierendes Design
In der Phase des Prototypings sollten die Prozesse der Massenproduktion berücksichtigt werden, wie z. B. Präzisionsspritzguss und 5-Achsen-Bearbeitung und es sollten angemessene Toleranzen festgelegt werden. Es ist nicht notwendig, extreme Präzision anzustreben, wenn die Anschlussmaße nicht kritisch sind . andernfalls steigen die Kosten für die Bearbeitung stark an. Designer müssen die Leistungsgrenzen verschiedener Prozesse verstehen und angemessene Spielräume für Herstellungsfehler lassen, während sie gleichzeitig die klinischen Anforderungen erfüllen.
Machbarkeit der Massenproduktion von Materialien und Oberflächenbehandlungen
Die Materialauswahl im Falle eines Prototyps sollte nicht nur die Anforderungen an Biokompatibilität und mechanische Eigenschaften erfüllen, sondern auch die Stabilität der Lieferkette und die Kosten in der Massenproduktion berücksichtigen. In der Zwischenzeit sollten spezielle Oberflächenbehandlungen, wie beispielsweise eine antibakterielle Beschichtung, stabil und gleichmäßig auf Teilechargen und nicht auf Laborproben angewendet werden können.
Ein erfolgreicher Prototyp eines chirurgischen Instruments berücksichtigt von Anfang an Überlegungen zur Herstellbarkeit . Es identifiziert und optimiert mögliche Fertigungs-, Qualitäts- und Kostenprobleme für die Großserienfertigung . Die Idee besteht darin, die Entwicklung eines „perfekten“ Produkts zu vermeiden, das entweder nicht herstellbar oder zu teuer in der Herstellung ist, und außerdem sicherzustellen, dass der Übergang vom Prototyp zur Massenproduktion reibungslos verläuft.
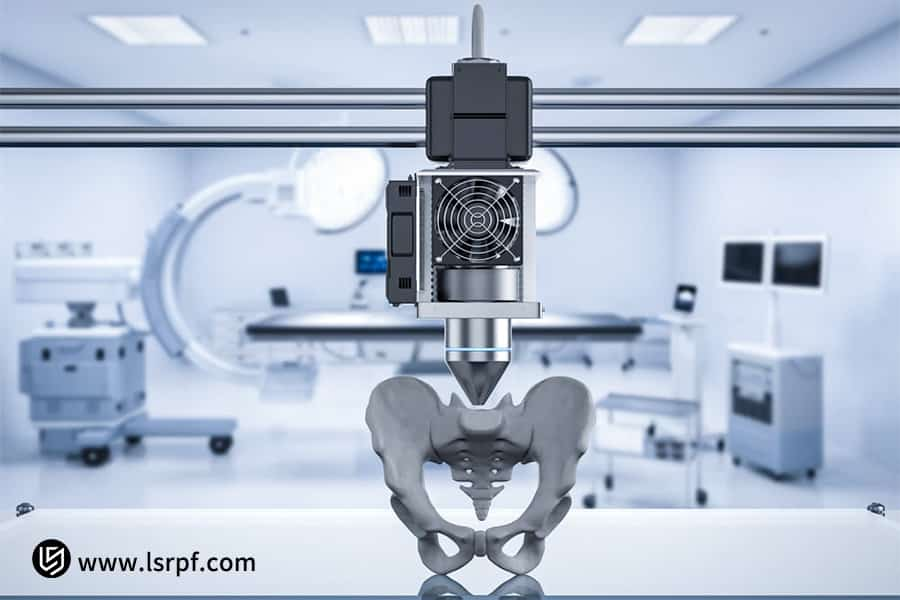
Abbildung 3: Beschleunigte Entwicklung maßgeschneiderter chirurgischer Implantate durch LS Manufacturing
Wie erleichtert die Rapid-Prototyping-Technologie Innovationen bei medizinischen Geräten?
Der wichtigste Wert von Rapid Prototyping für medizinische Geräte Der Vorteil liegt darin, dass es den Zeitraum vom Konzeptentwurf bis zur physischen Verifizierung verkürzen kann und eine sehr effektive Plattform für Versuch und Irrtum und Iteration bietet. Unter diesen Technologien spielt der 3D-Druck in medizinischer Qualität eine revolutionäre Rolle, wobei sich seine Vorteile und Anforderungen insbesondere in folgenden Punkten widerspiegeln:
- Komplexe Strukturen und individuelle Anpassung erreichen: Komplexe Mikrokanäle und poröse trabekuläre Knochenstrukturen, die mit herkömmlichen Methoden nur schwer zu verarbeiten sind, können mit 3D-Druck in medizinischer Qualität problemlos hergestellt werden. Dadurch können personalisierte Bohrschablonen und Implantate exakt an die Anatomie des Patienten angepasst hergestellt werden, eine Entwicklung, die direkt zur Präzisionsmedizin beiträgt.
- Integration mehrerer Materialien und Funktionen: Diese modernen Rapid-Prototyping-Technologien ermöglichen die Herstellung von Bauteilen aus einer Reihe von Materialien, die von starr über flexibel bis hin zu biologisch abbaubar reichen, alles in einem Bauteil. Beispielsweise kann eine integrierte Komponente, die ein starres Gerüst mit einer weichen Dichtung kombiniert, in einem Schritt gedruckt werden, um sie in anatomischen Modellen zu verwenden, die reale Organe oder Prototypen komplexer Arzneimittelverabreichungsgeräte simulieren.
- Erfüllung besonderer Anforderungen medizinischer Anwendungen: Sicherheit und Compliance dürfen beim Rapid Prototyping für medizinische Geräte niemals auf Kosten von Sicherheit und Compliance gehen , egal wie viel Geschwindigkeit auf dem Spiel steht. Materialien müssen biokompatibel sein und der Druckprozess selbst muss so validiert werden, dass er die Konsistenz von Charge zu Charge und die Rückverfolgbarkeit während des gesamten Prozesses gemäß den Anforderungen des Qualitätssystems gewährleistet.
Hierbei handelt es sich um eine Klasse von Rapid-Prototyping-Technologien, bei denen 3D-Druck in medizinischer Qualität ermöglicht es dem Forschungs- und Entwicklungsteam, bisher unmögliche Designs zu geringeren Kosten und in Rekordzeit zu erforschen. Die strenge Kontrolle von Materialien und Prozessen stellt sicher, dass Innovationen von der Anfangsphase bis zur klinischen Validierung und Produktregistrierung den konformen Weg gehen.
Wie hilft die LS-Herstellung minimalinvasiven chirurgischen Instrumenten, den technologischen Engpass zu überwinden?
Der Kernwert der Forschung und Entwicklung innovativer medizinischer Geräte, die wir anbieten, liegt darin Prototyping-Dienstleistungen für medizinische Geräte Wir helfen Kunden dabei, die wichtigsten technologischen Engpässe bei der Einführung ihrer Produkte zu überwinden. T Im Folgenden finden Sie eine typische Falldarstellung, die die Anwendung von demonstriert Medizinischer Prototyp von LS Manufacturing Ansatz:
Kundenherausforderung
Bei der Entwicklung eines neuartigen minimalinvasiven chirurgischen Instruments – einem intrakavitären Anastomosegerät – stieß ein innovatives Unternehmen bei Tierversuchen auf große Hindernisse. Der Kernübertragungsmechanismus zeigte eine erhebliche Verzögerung im Betrieb und konnte Chirurgen keine wirksame und präzise Kontrolle der Anastomosewirkung ermöglichen. Eingeschränkt durch den traditionellen Herstellungsprozess gab es aufgrund der komplizierten inneren Getriebestruktur keinen Raum mehr für weitere Optimierungen.
LS-Fertigungslösung
Unser Ingenieurteam hat daraufhin sofort die traditionelle Bearbeitungsmethode aufgegeben. Wir haben angestellt medizinischer Edelstahl 3D-Drucktechnologie zur Herstellung eines einstufigen und einteiligen Übertragungssystems mit einem überlegenen mechanischen Weg und extrem minimalem Spiel. Dadurch wurde nicht nur das Verzögerungsproblem gelöst; Eine weitere Verbesserung erfolgte durch Elektropolieren dieses komplexen, einteilig geformten Hohlraums , wodurch eine Oberflächenbeschaffenheit erzielt wurde, die weit über den Standards liegt und die extrem hohen Anforderungen an Sterilität und Sauberkeit für chirurgische Instrumente perfekt erfüllt.
Ergebnisse und Wert
In anschließenden Tierversuchen funktionierte der neu hergestellte Prototyp einwandfrei und die Reaktionsgeschwindigkeit und Genauigkeit des Instruments verbesserten sich um etwa 60 % , was von klinischen Experten großes Lob erhielt. Durch diesen technologischen Durchbruch konnte der Gesamtprojektzeitplan des Kunden direkt um mindestens fünf Monate verlängert und über 2 Millionen RMB an Forschungs- und Entwicklungskosten eingespart werden, die durch wiederholte Versuche und Formmodifikationen entstanden sind.
Wir haben fortschrittliche Technologien wie 3D-Druck in medizinischer Qualität eingesetzt, um gängige Struktur-, Material- und Leistungsbeschränkungen zu überwinden minimalinvasive chirurgische Instrumente für unsere Kunden. Was wie unmögliche technische Herausforderungen klang, wurde zum Schlüsselfaktor für die Wettbewerbsfähigkeit des Produkts und sicherte unseren Kunden wertvolle Time-to-Market-Fenster und enorme Kostenvorteile.

Abbildung 4: Präzisionsdosierung bei der Herstellung medizinischer Prototypen von LS Manufacturing
Welche technische Dokumentation ist für die Prototypenentwicklung bei Medizinprodukten erforderlich?
Voll technische Dokumentation ist der Grundstein für eine erfolgreiche Registrierung von Medizinprodukten. Es dient vor allem dazu, den Prozess der Designkontrolle umfassend zu dokumentieren und Nachweise über die Sicherheit und Wirksamkeit des Produkts zu erbringen. Dies dient nicht nur als Fahrplan für die interne Entwicklung, sondern dient den Aufsichtsbehörden auch als Beweis für die Fähigkeit des Unternehmens zur systematischen und konformen Entwicklung. Es muss unter anderem die folgenden Schlüsseldokumente enthalten:
- Design-Input- und Output-Dokumente: Dies ist der Beginn des Dokumentationssystems: Design-Inputs, die Benutzerbedürfnisse, klinische Funktionen, Leistungsindikatoren und regulatorische Standards klar aufzeichnen sollen. Zu den Designergebnissen gehören Produktzeichnungen, technische Spezifikationen, Teilelisten usw. Es sollte überprüft werden, dass jede Eingabe eine entsprechende Ausgabe hat.
- Materialzertifizierung und Biokompatibilitätsdokumentation: Lieferantenzertifizierungen und Materialzertifikate aller medizinischen Materialien sowie Biokompatibilitätsbewertungen oder Testberichte, soweit sie für Teile der USP-Klasse VI oder ISO 10993 relevant sind, sollten verfügbar sein. Dies steht in direktem Zusammenhang mit der Feststellung der Biokompatibilität des Produkts.
- Aufzeichnungen zur Validierung des Herstellungsprozesses: Zeigen Sie, dass der Herstellungsprozess des Prototyps für jeden kritischen Prozess, der an seiner Erstellung beteiligt ist, konsistent und kontrollierbar ist, z 3D-Druckparameter oder Sterilisationsprozesse , über detaillierte Prozessparameteraufzeichnungen, Gerätekalibrierungszertifikate und Erstmusterprüfberichte.
Mit anderen Worten bedeutet es, dass die Erstellung technischer Dokumentation als grundlegende Aktivität parallel zum Prototyping einen effizienten Projektfortschritt vorbereitet; es ist kein nachträglicher Einfall. Ein gutes Designkontrolle Ein Dokumentationssystem, beispielsweise die „Geburtsurkunde“ des Produkts, zeigt deutlich den Designverlauf vom Konzept bis zum Prototyp.
Wie plant man den Registrierungsantragspfad während der Prototyping-Phase?
Basierend auf der fundierten Vorbereitungsarbeit des Registrierungsantrags , Beschleunigung der Entwicklung medizinischer Geräte gewährleistet werden kann, und dabei sollen alle generierten Daten eine starke Stütze für künftige Zulassungsdokumente sein. Das heißt, die folgenden drei Ebenen sollten systematisch geplant werden:
Klare Definition der Anforderungen an den Registrierungsnachweis
Die Eingabephase des Prototypendesigns erfordert eine eingehende Analyse der regulatorischen Anforderungen des Zielmarkts. Hauptüberschriften, die bei der Prüfung von Registrierungen überprüft werden müssen, wie z. B. Leistungsindikatoren, Biokompatibilität und elektrische Sicherheit, werden in spezifische technische Parameter übersetzt, die durch den Prototyp überprüft werden. Dadurch wäre sichergestellt, dass die Entwicklung eines Prototyps von Anfang an auf dem richtigen Weg ist.
Wandeln Sie die Prototyp-Validierungsdaten in Registrierungsnachweise um
Der Prototyp muss Funktions-, Lebensdauer- und Benutzerfreundlichkeitstests unterzogen werden, die den Anforderungen des Qualitätssystems entsprechen. Alle Tests müssen mit einem vorab genehmigten Standardprotokoll durchgeführt werden, das eine vollständige Aufzeichnung der Rohdaten und einen standardisierten Bericht umfassen sollte. Hierbei handelt es sich um streng kontrollierte Daten, die dann direkt als Kernbeweis für die künftige Designvalidierung eingereicht werden können, wodurch wiederholte Tests vermieden werden.
Richten Sie ein transparentes System zur Dokumentation der Designhistorie ein
Es sollte eine vollständige Aufzeichnung des Prozesses von der Entwurfseingabe über die Überprüfung, Änderungen bis hin zur Ausgabe liefern. Dieses natürlich geformte Dokumentationssystem im Designkontrollprozess kann sich als der beste Beweis für die Aufsichtsbehörden erweisen, dass der Designprozess streng und kontrolliert ist, was die Effizienz und Erfolgsquote von Registrierungsprüfungen erheblich verbessern kann.
Mit anderen Worten: Planung Registrierungsantrag Die Integration in der Prototypenphase ist der beste Hebel zur Beschleunigung der Entwicklung medizinischer Geräte , da sie die hohen Kosten und Zeitverzögerungen, die in späteren Phasen des Projekts aufgrund zusätzlicher Registrierungsdaten entstehen, erheblich reduziert und gleichzeitig die Standardisierung und Erfolgsquote des gesamten F&E-Prozesses von Anfang an verbessert und so eine solide Grundlage für eine schnelle und stabile Markteinführung von Produkten legt
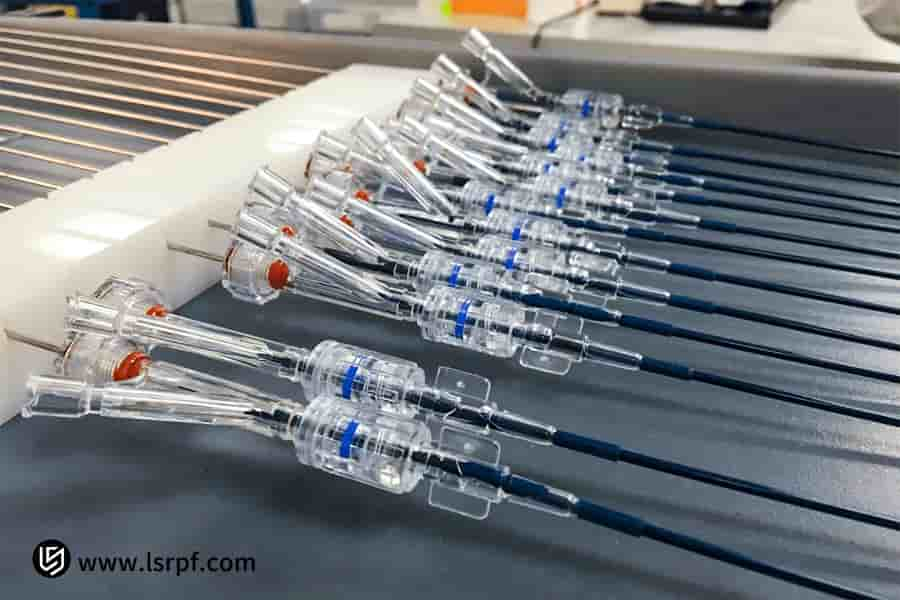
Abbildung 5: 360-Grad-Prototyp zur Funktionsvalidierung durch LS Manufacturing
FAQs
1. Welche spezifischen Anforderungen müssen bei der Entwicklung medizinischer Prototypengeräte beachtet werden?
Darüber hinaus muss man sich über die Grundfunktionalität hinaus proaktiv mit der Einhaltung der jeweiligen Standards für Medizinprodukte befassen. Wir wenden die konsequent an Qualitätssystem nach ISO 13485 um sicherzustellen, dass diese Prototypen gleich zu Beginn ihrer Registrierung die gesetzlichen Anforderungen in Bezug auf Biokompatibilität, Sterilisationstoleranz, elektrische Sicherheit und andere Aspekte erfüllen.
2. Wie lange dauert es vom Konzept bis zum ersten funktionsfähigen Prototypen?
Dies hängt von der Komplexität des Geräts ab. Relativ einfache Geräte benötigen etwa 2–3 Wochen, komplexere Geräte mit Präzisionsgetrieben und elektronischen Bauteilen hingegen 4–6 Wochen . Wir verfügen über einen beschleunigten Kanal, um dringenden Forschungs- und Entwicklungsbedarf flexibel zu decken und Ihren Projektzeitplan vollständig zu garantieren.
3. Ist es möglich, kleine Chargen von Geräten für klinische Studien herzustellen?
Zu unseren vielfältigen Dienstleistungen gehört natürlich auch die Herstellung kleiner Chargen von Geräten für klinische Studien , die zwischen 10 und 100 Einheiten umfassen. Die Herstellung erfolgte durch Herstellungsstandards für medizinische Geräte , und jede Einheit wird mit der anspruchsvollen Leistung, Qualität und Konsistenz für klinische Studien hergestellt.
4. Wie stellen Sie die Biokompatibilität von Prototypenmaterialien sicher?
Wir kontrollieren Risiken von der Quelle durch die strenge Auswahl medizinischer Materialien mit maßgeblichen Zertifizierungen wie ISO 10993 oder USP Class VI. Zusammen mit dem Prototyp können vollständige Materialzertifizierungsdokumente bereitgestellt werden, die einen wesentlichen Beweis für Ihre Biokompatibilitätsbewertung liefern.
5. Wie schützen Sie unser geistiges Eigentum während des Prototyping-Prozesses?
Informationssicherheit ist unsere Lebensader. Jedes Projekt beginnt mit einer rechtsverbindlichen Vertraulichkeitsvereinbarung und intern wenden wir ein striktes Datenhierarchie-Management- und Zugriffskontrollsystem an. Auf Wunsch des Kunden können auch physische und Informations-Firewalls eingerichtet werden.
6. Welche Art von Medizingeräte-Prototypen unterstützen Sie?
Die von unserem Unternehmen angebotenen Dienstleistungen reichen von aktiven Geräten wie Diagnosegeräten bis hin zu passiven Geräten wie chirurgischen Instrumenten, Implantaten und nicht implantierbaren Geräten . LS-Fertigung ist mit den Vorschriften und Prozessen verschiedener Produkte bestens vertraut.
7. Wie werden die Prototypendaten für die Verwendung in Anträgen auf spätere Registrierung verfügbar gemacht?
Neben Prototypen bieten wir ein komplettes Qualitätsnachweispaket, das detaillierte Produktionsaufzeichnungen, Prozessinspektionsberichte und Leistungstestdaten umfasst. Alle werden nach Spezifikationen erstellt und können direkt als Material zur Designüberprüfung zur Unterstützung von Registrierungsanträgen verwendet werden.
8. Wie startet man ein Prototypenprojekt für ein medizinisches Gerät?
Der Einstieg ist ganz einfach: Füllen Sie einfach einige erste Konzeptskizzen oder technische Anforderungen aus, und wir sorgen dafür, dass sich innerhalb eines Werktages ein leitender Ingenieur mit Ihnen in Verbindung setzt, um die technischen Lösungen eingehend zu besprechen und Ihnen eine erste Projektbewertung und ein Angebot zu unterbreiten.
Zusammenfassung
Prototypen medizinischer Geräte sind viel mehr als eine technische Realisierung; Sie sind der Eckpfeiler des Risikomanagements, der Einhaltung gesetzlicher Vorschriften und des kommerziellen Erfolgs. Die Suche nach dem richtigen Prototyping-Partner schafft eine solide Grundlage für den gesamten Produktlebenszyklus.
Wenn Sie also die Forschung und Entwicklung beschleunigen und gleichzeitig das Registrierungsrisiko verringern möchten, wenden Sie sich bitte an uns Kontaktieren Sie unsere Experten in Medizinprodukten für eine „Registrierungsorientierte Prototyping-Lösung“ für Ihr Projekt! Lassen Sie uns unsere Berufserfahrung in der Herstellung medizinischer Geräte nutzen, um Ihren Innovationsweg zu schützen.
📞Telefon: +86 185 6675 9667
📧E-Mail: info@longshengmfg.com
🌐Website: https://lsrpf.com/
Haftungsausschluss
Der Inhalt dieser Seite dient ausschließlich Informationszwecken. LS Manufacturing gibt keine Zusicherungen oder Gewährleistungen, weder ausdrücklich noch stillschweigend, hinsichtlich der Richtigkeit, Vollständigkeit oder Gültigkeit der Informationen. Daraus sollte nicht geschlossen werden, dass Drittanbieter oder Hersteller Leistungsparameter, geometrische Toleranzen, spezifische Designmerkmale, Materialqualität und -typ oder Prozesse über das LS Manufacturing-Netzwerk bereitstellen. Für diese Angaben ist ausschließlich der Käufer verantwortlich. Für Teileangebote geben Sie bitte die genauen Anforderungen für diese Teile an. Bitte kontaktieren Sie uns für weitere Informationen .
LS-Fertigungsteam
LS Manufacturing ist ein branchenführendes Unternehmen spezialisiert auf maßgeschneiderte Fertigungslösungen. Mit über 20 Jahren Erfahrung in der Betreuung von mehr als 5.000 Kunden legen wir Wert auf höchste Präzision CNC-Bearbeitung , Blechfertigung , 3D-Druck , Spritzguss , Metallstanzen und andere Fertigungsdienstleistungen aus einer Hand.
Unser Werk verfügt über mehr als 100 hochmoderne Fünf-Achsen-Bearbeitungszentren und ist nach ISO 9001:2015 zertifiziert. Wir bieten Kunden in über 150 Ländern und Regionen weltweit schnelle, effiziente und qualitativ hochwertige Fertigungslösungen. Ob Kleinserienfertigung oder Massenfertigung, wir können Ihre Anforderungen innerhalb von 24 Stunden erfüllen. Wenn Sie sich für LS Manufacturing entscheiden, entscheiden Sie sich für Effizienz, Qualität und Professionalität.
Weitere Informationen finden Sie auf unserer Website: www.lsrpf.com .