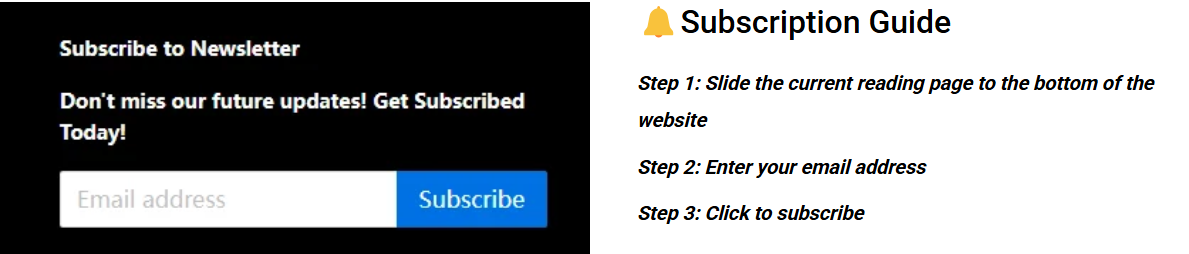
Прототип медицинского устройства Основная задача компании по обеспечению соответствия нормативным требованиям фундаментально отличается от общеинженерных прототипов. На самом деле, это основная причина заблуждений о медленной итерации. В традиционной модели она разделяет функциональную и нормативную проверку; таким образом, при столкновении с такими нормативными проблемами, как биосовместимость и электробезопасность, впоследствии приходится вносить радикальные модификации в прототип, что значительно задерживает клинические испытания и регистрацию.
Стратегия « Прототипирования, ориентированного на регистрацию » в LS Manufacturing систематически внедряет нормативные требования, начиная со стадии проектирования. Он ставит стандарты на первое место в своем списке приоритетов, чтобы обеспечить соответствие ключевым элементам регистрации в сочетании с функциональной реализацией прототипа, чтобы прототип был квалифицирован для клинической проверки и регистрационных испытаний, что обеспечивает первый успех при запуске продукта. Чтобы сэкономить ваше время, ниже представлен краткий обзор основных выводов.
Краткое руководство по прототипированию медицинского оборудования
| Модуль | Ключевой вывод |
| Основная концепция | Создавайте « прототипы, ориентированные на регистрацию », которые включают в себя функции, соответствующие нормативным требованиям. |
| Традиционные болевые точки | Введение нормативных требований на поздних стадиях процесса приводит к повторным модификациям прототипа, что затягивает время выхода на рынок. |
| Ключевые элементы | Биосовместимость, удобство использования и управление рисками должны рассматриваться все вместе на этапе прототипирования. |
| Решение | Получите правильный проект с первого раза благодаря активному надзору со стороны регулирующих органов и параллельной работе. |
| Конечная ценность | Значительное снижение риска регистрации и существенное сокращение общего цикла запуска продукта. |
В следующей таблице показано, как ускорить разработку медицинского оборудования . путем изменения нормативных требований от «препятствия поздней стадии» к «вкладам в проектирование на ранней стадии». Движение к «регистрационно-ориентированному» подходу означает, что сам прототип станет основой для регистрации, без разрушительных модификаций в дальнейшем, с целью эффективного, надежного и быстрого вывода на рынок.
Почему стоит доверять этому руководству? Практический опыт экспертов LS Manufacturing
В Интернете есть несколько тысяч статей на тему прототипирования медицинских устройств. Так зачем же вам тратить время на чтение этой статьи? То, чем мы здесь делимся, взято не из определения из учебника, а скорее из некоторых практических рекомендаций, связанных строгими ограничениями стандарта ISO 13485 и ИСО9001 системы и подтверждено бесчисленными операциями и результатами испытаний.
За более чем десять лет наша команда изготовила более 50 000 индивидуальных прототипов, соответствующих ISO 13485 для медицинского оборудования Требования к системе качества. Каждый проект давал нам более глубокое понимание того, как задавать параметры резки биоразлагаемых магниевых сплавов без термического повреждения, как сохранять стабильность тонкостенных конструкций при микрофрезеровании и как одновременно реализовывать требования управления рисками и проектирования удобства использования на каждом этапе итерации.
Поверьте нам, то, что вы здесь читаете, — это основная методология, которую мы используем ежедневно для решения проблем. Давайте работать вместе, чтобы эффективно и надежно превратить ваши новые идеи в заслуживающие доверия продукты.

Рисунок 1. Комплексный прототип для проверки функциональности от LS Manufacturing.
Почему прототипы медицинских устройств должны выходить за рамки «функциональной проверки»?
Конечная цель прототипа медицинского устройства — стать не просто «работающей» моделью, а « прототипом продукта », способным пройти все сложные процессы регистрации и утверждения и безопасно применяться на человеческом теле. Следовательно, объем его валидации должен включать полный жизненный цикл рисков использования.
- Толерантность к стерильности: прототип может иметь идеальную двигательную функцию, но не может выдерживать повторяющиеся процессы стерилизации, такие как высокие температуры и давления, облучение или химическое погружение . Старение материала может ухудшить его характеристики и вызвать клиническую инфекцию. Соответствующие материалы должны быть выбраны и проверены на стадии прототипа .
- Обзор биосовместимости: Детали, вступающие в прямой или косвенный контакт с пациентами , должны быть изготовлены из нетоксичных и неаллергенных материалов . Такая замена биосовместимыми материалами на более поздних стадиях процесса проектирования может повлиять на их механические свойства и потребовать полной структурной перестройки.
- Безопасность и ЭМС (электромагнитная совместимость). В случае активных устройств прототипы должны заранее учитывать электрическую изоляцию, ток утечки и другие показатели безопасности, чтобы во время работы избежать влияния на другое оборудование без влияния внешних помех. За последующее исправление приходится платить астрономически высокую цену, и с этим приходится сталкиваться при регистрации и тестировании.
Внедрение требований соответствие нормативным требованиям Разработка прототипов медицинских устройств на самом деле является упреждающим подходом к управлению рисками. Это позволит избежать радикальных изменений конструкции из-за проблем с функциональностью, возникающих во время регистрации и тестирования или клинической проверки, что существенно сэкономит много времени и денег, а также послужит краеугольным камнем для ускорения запуска продукта .
Как сертификация ISO 13485 влияет на систему качества при разработке прототипов?
Прототип ISO 13485 превращает процесс из потенциально случайной деятельности в контролируемый, отслеживаемый и жизненно важный процесс , который обеспечивает раннюю уверенность в безопасности и эффективности конечного продукта. Это требует наличия надежной системы качества , начиная с этапа разработки концепции. Особенно это отражается в:
Строгий контроль проектирования и управление документацией
Для прототипирования необходимо иметь документацию по вводу, выводу, проверке и изменениям проекта в соответствии со стандартом ISO 13485. Требуются полностью документированные спецификации, от спецификаций требований заказчика до протоколов изменений чертежей и заключений по результатам проверки проекта. Это также обеспечивает согласованность между прототипом и замыслом проекта и формирует полезную «историю проектирования», предоставляя прямые доказательства для последующих заявок на регистрацию.
Контролируемое производство и отслеживание
Этот стандарт требует проверки и контроля ключевых процессов прототипирования. Например, в отношении материалов медицинского назначения должны быть предоставлены квалификационные сертификаты поставщика и записи входного контроля ; это также включает в себя настройку и подтверждение параметров технологического оборудования, таких как толщина слоя и мощность лазера в 3D-печать . Это обеспечит последовательность и повторяемость в этом процессе прототипирования и дают четкую основу для будущего репликации или итерации.
Ранняя интеграция управления рисками
Деятельность по управлению рисками должна начинаться достаточно рано во время прототипирования, чтобы выявить потенциальные риски, связанные с конструкцией, материалами и процессами, для которых следует принять меры контроля. В этом отношении это заставляет команду заранее думать о требованиях, связанных с безопасностью, таких как очистка, стерилизация и биосовместимость , интегрировать решения в проектирование и производство прототипа , снижая вероятность серьезных изменений конструкции в дальнейшем.
Значение, исходящее из система качества Весь процесс создания прототипа выходит далеко за рамки простого получения сертификата ISO 13485 . Это создаст для самого прототипа стандартизированную и прозрачную структуру ; не только функциональный «образец», но и надежный, полный данных и контролируемый риск « предварительный продукт ».
Выбор материалов медицинского назначения, отвечающих требованиям биосовместимости?
Отбор является первым препятствием в определении биосовместимости и безопасности продукта при разработке прототипа медицинского устройства . Выбор подходящего материала минимизирует риски при регистрации, но, самое главное, обеспечивает безопасность пациента. Чтобы прояснить логику выбора, ниже сравниваются ключевые соображения.
| Размеры рассмотрения | Основной путь: выбор сертифицированных материалов |
Продвинутый путь: биологическая оценка материалов |
| Принцип | Использование материалы медицинского назначения на первом месте стоит зрелая сертификация, такая как USP Class VI или ISO 10993. | Если используется инновационный материал, потребуется полная биологическая оценка в соответствии со стандартами ISO 10993 . |
|
Применимые сценарии |
Применяется к большинству зрелых материалов с низким риском и имеющим четкий и быстрый маршрут. | Применяется к новым, инновационным материалам или совершенно новым сценариям взаимодействия человека с человеком, сопряженным с более высоким риском и затратами. |
| Ключевые доказательства | Полностью заполненные сертификаты сертификации и протоколы испытаний от поставщика материала. |
Ввод в эксплуатацию правильно оборудованной и квалифицированной лаборатории для проведения полного или частичного комплекса необходимых испытаний на безопасность. |
| Наша поддержка | Мы обеспечиваем быстрый подбор и рекомендации на основе проверенной базы данных материалов медицинского назначения , а также консультации по схемам оценки и поддержку тестирования. | Мы поддерживаем клиентов в снижении рисков, связанных с соблюдением требований, на протяжении всего процесса. |
Мы настоятельно рекомендуем планировать биосовместимость прямо на ранних этапах создания прототипа, выбирая предварительно сертифицированные материалы из проверенных баз данных, чтобы минимизировать неопределенность . Там, где необходимо удовлетворить инновационные потребности, полный путь биологической оценки будет запланирован задолго до этого. Это позволит избежать задержек в регистрации и сбоев в разработке проектов из-за материальных проблем с самого начала и заложит основу для безопасности и быстрого вывода продукции на рынок.

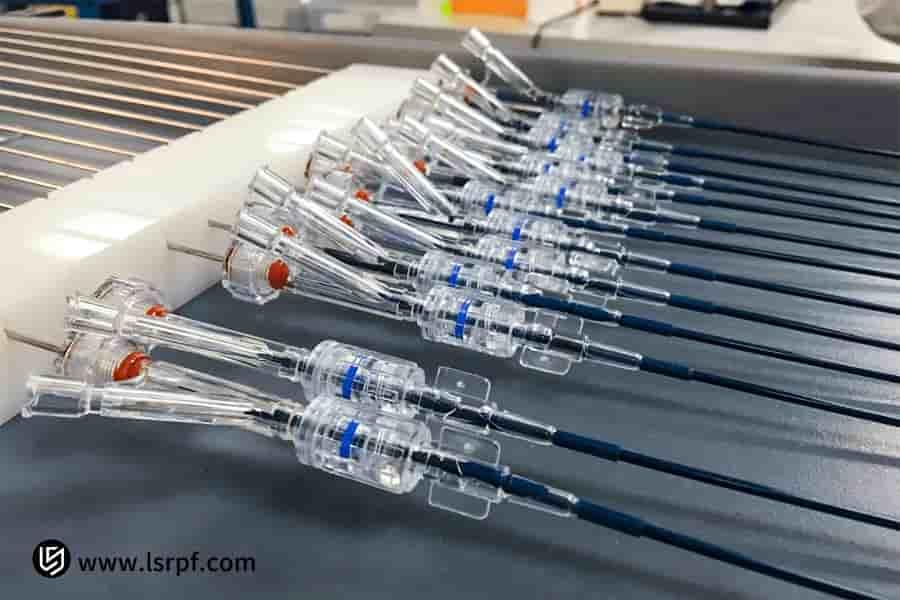
Рисунок 2: Точный объемный контроль медицинских прототипов от LS Manufacturing.
Каким стандартам должны соответствовать прототипы на разных клинических стадиях?
Большинство людей неверно истолковывают прототипирование медицинских устройств как деятельность, в которой одна версия прототипа пытается удовлетворить все потребности. Это часто приводит к напрасной трате ресурсов при использовании или отсутствию стандартов. Наука точно поддерживает на каждом этапе – от концепции до клинической проверки – создание «правильных» прототипов, основанных на целях различных клинических стадий.
| Клиническая стадия | Прототипируйте основные цели | Производственные стандарты и стратегии |
| Доказательство концепции | Как можно скорее проверьте осуществимость проектной концепции. | Экономичные и быстрые методы, такие как 3D-печать, позволяют достичь основных функций. Материалы безграничны; сейчас настало время для быстрой итерации. |
| Функциональное тестирование |
Проводить комплексные инженерные испытания прототипов. |
Тщательная проверка производительности и надежности продукта с использованием прототипов, которые точно отражают размер продукта, материалы и характеристики. |
| Тестирование на животных | Первым шагом процедуры является оценка безопасности рассматриваемого продукта и его биосовместимости . | Он должен быть приготовлен из биосовместимого материала медицинского назначения после асептической обработки, чтобы результаты испытаний были действительными. |
| Клиническая проверка | Данные о безопасности и эффективности должны быть получены в ходе испытаний, проводимых на людях. | Прототип должен представлять собой конечный продукт и соответствовать нормы медицинского оборудования в отношении производительности, материалов и производственных процессов. |
Вообще говоря, прототипирование медицинских устройств эффективно работает при динамичном, но прогрессивном подходе. От «экономной» стадии проверки концепции до стадии «квазикоммерциализации» , с клиническая валидация На каждом этапе проектирования прототипа должны быть поставлены определенные цели, соответствующие стандартам. Такая стратегия позволит эффективно контролировать затраты на НИОКР на ранних стадиях, обеспечивая при этом целостность и надежность цепочки данных прототипа , тем самым позволяя избежать задержек или сбоев проекта из-за несоответствия стандартов прототипа.
Как можно сбалансировать точность и технологичность в прототипе хирургических инструментов?
В процессе прототип хирургических инструментов Целью разработки является не только достижение большей функциональной точности, но и доказательство того, что его конструкция может быть стабильно и экономично преобразована в качественную продукцию массового производства. Принципам проектирования с учетом технологичности следует уделять приоритетное внимание. Поэтому необходимо учитывать следующие моменты:
Структурное упрощение и оптимизация сборки
При обеспечении функциональности следует свести к минимуму количество деталей и избегать сложных внутренних конструкций. Например, вместо традиционных сборочных конструкций, состоящих из нескольких частей, можно использовать интегрированную технологию 3D-печати или вместо винтового крепления можно использовать самоблокирующиеся конструкции с защелками . При этом можно значительно сократить трудности и время последующей сборки, что повышает эффективность и стабильность производства.
Согласование производственных процессов и проектирование с учетом допусков
На этапе прототипирования следует учитывать процессы массового производства, такие как прецизионное литье под давлением и 5-осевая обработка и должны быть установлены разумные допуски. Нет необходимости добиваться предельной точности, если сопрягаемые размеры не являются критическими ; в противном случае стоимость переработки резко возрастет. Разработчикам необходимо понимать границы возможностей различных процессов и оставлять разумные пределы для производственных ошибок, одновременно соблюдая клинические требования.
Целесообразность массового производства материалов и обработки поверхности
Выбор материала в случае прототипа должен отвечать не только требованиям биосовместимости и механических свойств, но также учитывать стабильность цепочки поставок и стоимость при массовом производстве. Между тем, специальная обработка поверхности, такая как антибактериальное покрытие, должна иметь возможность стабильно и равномерно применяться к партиям деталей, а не к лабораторным образцам.
Успешный прототип хирургического инструмента с самого начала учитывает соображения технологичности . Он выявляет и оптимизирует возможные проблемы производства, качества и затрат для крупномасштабного производства . Идея состоит в том, чтобы избежать разработки «идеального» продукта, который либо невозможно произвести, либо сделать слишком дорого, а также обеспечить плавный переход от прототипа к массовому производству.
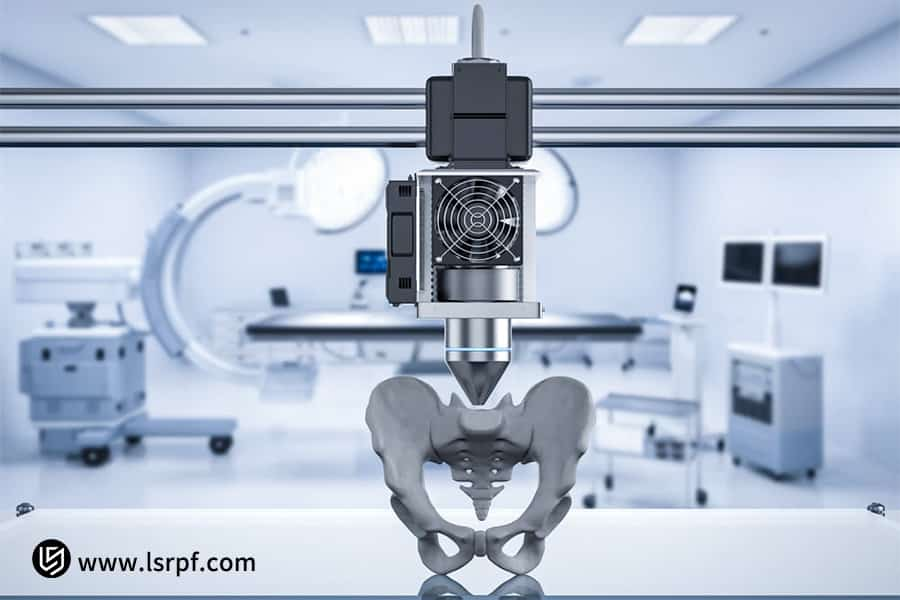
Рисунок 3. Ускоренная разработка индивидуальных хирургических имплантатов компанией LS Manufacturing.
Как технология быстрого прототипирования способствует инновациям в медицинских устройствах?
Самая главная ценность быстрое прототипирование медицинских устройств заключается в том, что он может сократить период времени от концептуального проектирования до физической проверки, предоставляя очень эффективную платформу для проб и ошибок и итераций. Среди этих технологий 3D-печать медицинского уровня играет революционную роль, ее преимущества и требования особенно отражены в:
- Создание сложных структур и индивидуальная настройка: сложные микроканалы и пористые структуры трабекулярной кости, которые трудно обрабатывать традиционными методами, можно легко изготовить с помощью 3D-печати медицинского уровня . Таким образом, персонализированные хирургические шаблоны и имплантаты могут быть изготовлены так, чтобы они точно соответствовали анатомии пациента, и эта разработка напрямую способствует прецизионной медицине.
- Интеграция нескольких материалов и функций: эти современные технологии быстрого прототипирования позволяют изготавливать компоненты из различных материалов, от жестких и гибких до биоразлагаемых, и все это в одном компоненте. Например, интегрированный компонент, сочетающий жесткий каркас с мягким уплотнением, можно распечатать за один этап и использовать в анатомических моделях, имитирующих реальные органы или прототипы сложных устройств для доставки лекарств.
- Соответствие особым требованиям медицинских приложений. При быстром создании прототипов медицинских устройств никогда нельзя жертвовать безопасностью и соответствием требованиям , независимо от того, насколько скорость поставлена на карту. Материалы должны быть биосовместимыми, а сам процесс печати должен быть проверен таким образом, чтобы обеспечить единообразие от партии к партии и отслеживаемость на протяжении всего процесса в соответствии с требованиями системы качества .
Это класс технологий быстрого прототипирования, в которых 3D-печать медицинского уровня позволяет команде исследований и разработок исследовать ранее невозможные конструкции с меньшими затратами и в рекордно короткие сроки. Строгий контроль над материалами и процессами гарантирует, что инновации будут соответствовать требованиям, начиная с начальной стадии и заканчивая клинической проверкой и регистрацией продукта.
Как производство LS помогает минимально инвазивным хирургическим инструментам преодолеть технологические узкие места?
Основная ценность исследований и разработок инновационных медицинских устройств, которые мы предлагаем, связана с их услуги по прототипированию медицинского оборудования помогая клиентам преодолеть ключевые технологические препятствия при запуске их продуктов. Т Ниже приводится типичная иллюстрация случая, демонстрирующая применение LS Производство медицинского прототипа подход:
Клиентский вызов
В процессе разработки нового вида малоинвазивного хирургического инструмента — устройства для внутриполостного анастомоза — инновационная компания столкнулась с огромными препятствиями при испытаниях на животных. Механизм основной передачи демонстрировал значительное отставание в работе и не мог обеспечить хирургам эффективный и точный контроль действия анастомоза. Ограниченный традиционным производственным процессом, возможности для дальнейшей оптимизации больше не было из-за сложной внутренней структуры трансмиссии.
Производственное решение LS
Вмешавшись, наша команда инженеров немедленно отказалась от традиционного метода обработки. Мы наняли медицинская нержавеющая сталь Технология 3D-печати , позволяющая производить одноступенчатую и цельную систему передачи с превосходным механическим путем и предельно минимальным зазором. Это не только решило проблему отставания; Дальнейшее усовершенствование заключалось в применении электрополировки к этой сложной цельной формованной полости , что придало ей качество поверхности, намного превосходящее стандартное, и полностью отвечающее чрезвычайно высоким требованиям стерильности и чистоты хирургических инструментов.
Результаты и ценность
В последующих испытаниях на животных вновь изготовленный прототип работал отлично, а скорость реагирования и точность инструмента улучшились примерно на 60% , завоевав высокую оценку клинических экспертов. Таким образом, этот технологический прорыв продвинул общий график проекта клиента как минимум на 5 месяцев и сэкономил более 2 миллионов юаней на затратах на исследования и разработки, понесенных в результате повторных проб и ошибок и модификаций пресс-форм.
Мы применили передовые технологии, такие как 3D-печать медицинского уровня, чтобы преодолеть общие ограничения по структуре, материалам и производительности. малоинвазивные хирургические инструменты для наших клиентов. То, что казалось невыполнимыми техническими задачами, стало ключевой конкурентоспособностью продукта, обеспечивая ценные сроки выхода на рынок и огромные финансовые преимущества для наших клиентов.

Рисунок 4. Точное дозирование при изготовлении медицинских прототипов компанией LS Manufacturing.
Какой тип технической документации требуется для разработки прототипа медицинского оборудования?
Полный техническая документация является краеугольным камнем успешной регистрации медицинского оборудования. Он служит главным образом для всестороннего документирования процесса контроля конструкции и предоставления доказательств безопасности и эффективности продукта. Это будет не только дорожной картой для внутреннего развития, но также послужит регулирующим органам доказательством способности предприятия к систематическому и соответствующему развитию. Он должен включать, помимо прочего, следующие ключевые документы:
- Входные и выходные документы проектирования: это начало системы документации: входные данные проектирования, которые должны четко фиксировать потребности пользователей, клинические функции, показатели эффективности и нормативные стандарты. Результаты проектирования будут включать чертежи продукта, технические характеристики, списки деталей и т . д. Каждый вход должен быть проверен на наличие соответствующего выхода.
- Сертификация материалов и документация о биосовместимости. Должны быть доступны сертификаты поставщиков и сертификаты материалов на все материалы медицинского назначения вместе с оценкой биосовместимости или отчетами об испытаниях, соответствующими частям класса VI USP или ISO 10993. Это напрямую связано с установлением биосовместимости продукта.
- Записи о проверке производственного процесса. Продемонстрируйте, что процесс производства прототипа является последовательным и контролируемым для каждого критического процесса, участвующего в его создании, например: Параметры 3D-печати или процессов стерилизации , посредством подробных записей параметров процесса, сертификатов калибровки оборудования и отчетов о проверке первого изделия.
Другими словами, это означает создание технической документации как основной деятельности, которая выполняется параллельно с прототипированием и подготавливает к эффективному развитию проекта; это не запоздалая мысль. Хороший контроль проектирования Система документации, такая как «свидетельство о рождении» продукта, четко показывает траекторию проектирования от концепции до прототипа.
Как спланировать путь подачи заявки на регистрацию на этапе прототипирования?
На основании тщательной подготовки заявки на регистрацию , ускорить разработку медицинского оборудования могут быть гарантированы, и в этом процессе каждая полученная часть данных станет надежной поддержкой для будущих регистрационных документов. Иными словами, необходимо систематически планировать следующие три уровня:
Четкое определение требований относительно доказательств регистрации
Этап разработки прототипа требует углубленного анализа нормативных требований целевого рынка. Основные заголовки, которые необходимо проверить при проверке регистрации, такие как показатели эффективности, биосовместимость и электробезопасность, переводятся в конкретные технические параметры, подлежащие проверке по прототипу. Это обеспечит разработку прототипа в правильном направлении с самого начала.
Преобразуйте данные проверки прототипа в регистрационные доказательства
Прототип должен пройти функциональные испытания, испытания на срок службы и удобство использования, соответствующие требованиям системы качества . Все тесты должны проводиться по заранее утвержденному стандартному протоколу, который должен включать полную запись необработанных данных и стандартизированный отчет. Это будут строго контролируемые данные, которые затем можно будет напрямую представить в качестве основного доказательства для будущей проверки проекта, что позволит избежать повторных испытаний.
Создать прозрачную систему документации по истории проектирования.
Он должен обеспечивать полную запись процесса, начиная с входных данных проекта и заканчивая анализом, изменениями и выходными данными. Эта естественно сформированная система документации в процессе контроля проектирования может оказаться лучшим доказательством, подтверждающим регулирующим органам, что процесс проектирования является строгим и контролируемым, что может значительно повысить эффективность и успешность регистрационных проверок.
Другими словами, планирование заявка на регистрацию интеграция на этапе прототипа является лучшим рычагом для ускорения разработки медицинского оборудования , поскольку она значительно сокращает высокие затраты и временные задержки, возникающие на более поздних этапах проекта из-за дополнительных регистрационных данных, одновременно улучшая стандартизацию и уровень успеха всего процесса исследований и разработок с самого начала, закладывая прочную основу для быстрого и стабильного вывода продукции на рынок.
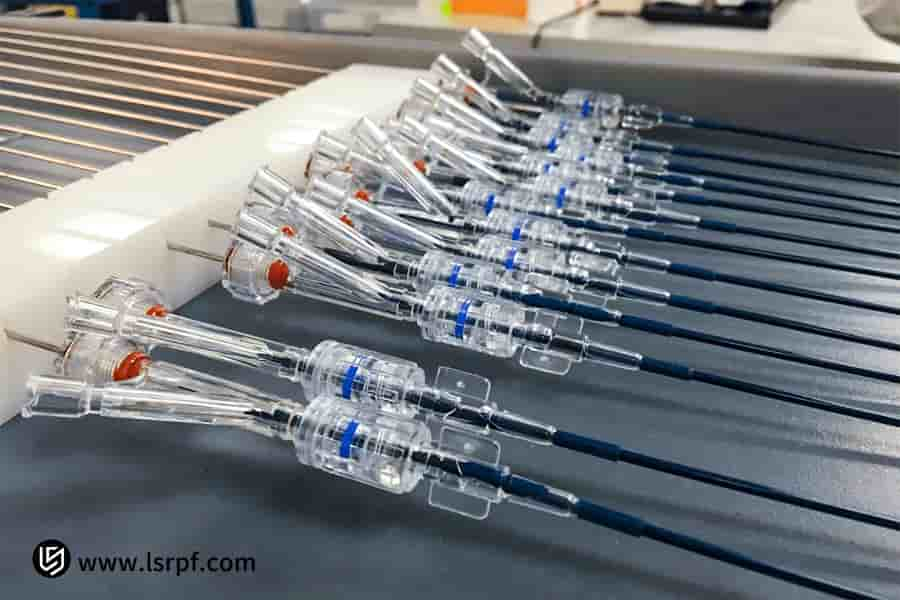
Рисунок 5. Прототип с обзором на 360 градусов для функциональной проверки LS Manufacturing.
Часто задаваемые вопросы
1. Какие конкретные требования необходимо соблюдать при разработке медицинских прототипов изделий?
Кроме того, помимо базовой функциональности, необходимо активно решать вопросы соблюдения конкретных стандартов для медицинских устройств. Мы строго применяем система качества ISO 13485 обеспечить соответствие этих прототипов нормативным требованиям по биосовместимости, стерилизации, электробезопасности и другим аспектам уже в самом начале их регистрации.
2. Сколько времени проходит от концепции до получения первого функционального прототипа?
Это зависит от сложности устройства. Сравнительно простые устройства занимают около 2-3 недель, а более сложные с прецизионными трансмиссиями и электронными компонентами — 4-6 недель . У нас есть ускоренный канал для гибкого решения неотложных потребностей в исследованиях и разработках и полная гарантия графика вашего проекта.
3. Возможно ли изготовление небольших партий устройств для клинических испытаний?
Конечно, одна из наших разнообразных услуг — это изготовление небольших партий устройств для клинических испытаний , от 10 до 100 единиц . Производство осуществлялось стандарты производства медицинского оборудования , и каждое устройство будет изготовлено с учетом требований к производительности, качеству и стабильности для клинических испытаний.
4. Как обеспечивается биосовместимость материалов-прототипов?
Мы контролируем риски от источника посредством строгого отбора материалов медицинского назначения, имеющих такие авторитетные сертификаты , как ISO 10993 или USP Class VI. Вместе с прототипом могут быть предоставлены полные документы по сертификации материалов, что предоставит существенные доказательства для вашей оценки биосовместимости.
5. Как вы защищаете нашу интеллектуальную собственность в процессе создания прототипа?
Информационная безопасность – наша линия жизни. Каждый проект начинается с юридически обязывающего соглашения о конфиденциальности, а внутри компании мы применяем строгую систему управления иерархией данных и контроля доступа. По желанию клиента также могут быть установлены физические и информационные межсетевые экраны.
6. Какие типы прототипов медицинского оборудования вы поддерживаете?
Услуги, предлагаемые нашей компанией, варьируются от активных устройств, таких как диагностическое оборудование, до пассивных, включая хирургические инструменты, имплантаты и неимплантируемые устройства . ЛС Производство хорошо разбирается в правилах и процессах, связанных с различными продуктами.
7. Как сделать данные прототипа доступными для использования в заявках на последующую регистрацию?
Помимо прототипов, мы предоставляем полный пакет доказательств качества, который включает подробные производственные записи, отчеты о проверке технологического процесса и данные испытаний производительности . Все они создаются в соответствии со спецификациями и могут быть непосредственно использованы в качестве материала для проверки конструкции для поддержки заявок на регистрацию.
8. Как начать проект прототипа медицинского устройства?
Процесс начала довольно прост: просто заполните несколько первоначальных концептуальных эскизов или технических требований, и мы позаботимся о том, чтобы старший инженер свяжется с вами в течение одного рабочего дня, чтобы подробно обсудить технические решения и предоставить вам первоначальную оценку проекта и коммерческое предложение.
Краткое содержание
Прототипы медицинских устройств — это нечто большее, чем просто техническая реализация; они являются краеугольным камнем управления рисками, соблюдения нормативных требований и коммерческого успеха. Поиск подходящего партнера по прототипированию закладывает прочную основу для всего жизненного цикла продукта.
Поэтому, если вы хотите ускорить НИОКР и одновременно снизить риски регистрации, пожалуйста, свяжитесь с нашими экспертами в медицинских устройствах сегодня для «Решения для прототипирования, ориентированного на регистрацию» для вашего проекта! Позвольте нам применить наш профессиональный опыт в производстве медицинского оборудования, чтобы защитить ваш путь к инновациям.
📞Телефон: +86 185 6675 9667.
📧Электронная почта: info@longshengmfg.com
🌐Сайт: https://lsrpf.com/
Отказ от ответственности
Содержимое этой страницы предназначено только для информационных целей. LS Manufacturing не делает никаких заявлений и не дает никаких гарантий, явных или подразумеваемых, относительно точности, полноты или достоверности информации. Не следует предполагать, что сторонние поставщики или производители будут предоставлять параметры производительности, геометрические допуски, конкретные конструктивные характеристики, качество и тип материала или процессы через производственную сеть LS. Покупатель несет полную ответственность за эту информацию. Для получения цен на детали укажите точные требования к этим деталям. Пожалуйста, свяжитесь с нами для получения дополнительной информации .
Производственная группа LS
LS Manufacturing — ведущая компания отрасли. специализируется на индивидуальных производственных решениях. Обладая более чем 20-летним опытом обслуживания более 5000 клиентов, мы уделяем особое внимание высокоточным обработка с ЧПУ , изготовление листового металла , 3D-печать , литье под давлением , штамповка металла и другие универсальные производственные услуги.
Наш завод располагает более чем 100 современными пятиосными обрабатывающими центрами и сертифицирован по стандарту ISO 9001:2015. Мы предоставляем быстрые, эффективные и высококачественные производственные решения клиентам в более чем 150 странах и регионах по всему миру. Будь то мелкосерийное производство или массовая индивидуализация, мы можем удовлетворить ваши потребности в течение 24 часов. Выбор LS Manufacturing означает выбор эффективности, качества и профессионализма.
Для получения дополнительной информации посетите наш сайт: www.lsrpf.com .