Prototipo di dispositivo medico La missione principale di garantire la conformità normativa è fondamentalmente diversa dai prototipi di ingegneria generale. In realtà, questa è la causa principale di idee sbagliate sull'iterazione lenta. Nel modello tradizionale si separa la verifica funzionale da quella normativa; pertanto, quando si affrontano sfide normative come la biocompatibilità e la sicurezza elettrica, è necessario apportare successivamente modifiche drastiche al prototipo, ritardando enormemente le sperimentazioni cliniche e la registrazione.
La strategia di " Prototipazione orientata alla registrazione " di LS Manufacturing incorpora i requisiti normativi in modo sistematico fin dalla fase di progettazione. Pone gli standard in cima alla sua lista di priorità per garantire il rispetto degli elementi chiave di registrazione insieme alla realizzazione funzionale del prototipo, in modo tale che il prototipo sia qualificato per la validazione clinica e i test di registrazione, garantendo così il primo successo nel lancio del prodotto. Per farti risparmiare tempo, ecco una breve panoramica dei principali risultati.
Guida rapida per la prototipazione di dispositivi medici
| Modulo | Chiave da asporto |
| Concetto fondamentale | Crea " prototipi orientati alla registrazione " che incorporino la funzionalità con la conformità normativa. |
| Punti dolenti tradizionali | L'introduzione di requisiti normativi in una fase avanzata del processo comporta ripetute modifiche al prototipo, ritardando il time-to-market. |
| Elementi chiave | La biocompatibilità, l'ingegneria dell'usabilità e la gestione del rischio devono essere affrontate tutte insieme nella fase di prototipazione. |
| Soluzione | Ottieni la progettazione corretta fin dal primo momento attraverso una supervisione normativa proattiva e lavorando in parallelo. |
| Valore ultimo | Riducendo drasticamente il rischio di registrazione e abbreviando sostanzialmente il ciclo totale di lancio del prodotto. |
La tabella seguente illustra come accelerare lo sviluppo di dispositivi medici spostando i requisiti normativi da "ostacolo in fase avanzata" a "input di progettazione in fase iniziale". Il movimento verso un approccio “orientato alla registrazione” significa che il prototipo stesso diventerà la base per la registrazione, senza modifiche dirompenti successive, con l’obiettivo di un lancio sul mercato efficiente, affidabile e rapido.
Perché fidarsi di questa guida? Esperienza pratica da parte di esperti di produzione LS
Esistono diverse migliaia di articoli online riguardanti l'argomento della prototipazione di dispositivi medici, quindi perché dovresti dedicare il tuo tempo a leggere questo? Ciò che condividiamo qui non proviene da una definizione da libro di testo ma piuttosto da alcune linee guida pratiche vincolate dai rigorosi vincoli della norma ISO 13485 e ISO9001 sistema e convalidato attraverso innumerevoli interventi chirurgici e risultati di test.
Per oltre un decennio, il nostro team ha prodotto più di 50.000 prototipi personalizzati che soddisfano i requisiti ISO 13485 per i dispositivi medici requisiti del sistema qualità. Ciascun progetto ci ha fornito una comprensione più approfondita di come impostare i parametri di taglio per le leghe di magnesio biodegradabili senza danni termici, di come mantenere la stabilità nelle strutture a pareti sottili durante la microfresatura e di come implementare contemporaneamente i requisiti di gestione del rischio e ingegneria dell'usabilità in ogni fase dell'iterazione.
Fidati di noi, quello che leggi qui è la metodologia fondamentale che utilizziamo quotidianamente per superare le sfide. Lavoriamo insieme per trasformare le vostre nuove idee con efficienza e affidabilità in prodotti affidabili.

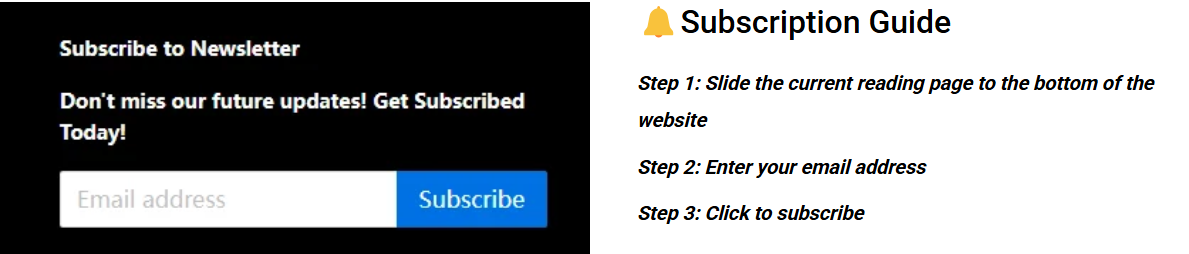
Figura 1: Prototipo completo per la verifica della funzionalità da parte di LS Manufacturing
Perché i prototipi dei dispositivi medici dovrebbero andare oltre la “convalida funzionale”?
L'obiettivo finale del prototipo del dispositivo medico non è solo quello di essere un modello "funzionante", ma un " prototipo di prodotto " in grado di superare tutti i severi processi di registrazione e approvazione e di essere applicato in sicurezza sul corpo umano. Pertanto, l’ambito della sua convalida deve includere l’intero ciclo di vita dei rischi d’uso.
- Tolleranza alla sterilità: un prototipo potrebbe avere una funzione motoria perfetta ma potrebbe non sopportare ripetuti processi di sterilizzazione, come temperature e pressioni elevate, irradiazione o immersione chimica . L'invecchiamento del materiale può ridurne le prestazioni e causare infezioni cliniche. I materiali conformi devono essere selezionati e validati durante la fase di prototipo .
- Panoramica sulla biocompatibilità: Le parti che entrano in contatto diretto o indiretto con i pazienti devono essere realizzate con materiali atossici e anallergici . Questa sostituzione con materiali biocompatibili in una fase successiva del processo di progettazione potrebbe influenzarne le proprietà meccaniche e richiedere una riprogettazione strutturale completa.
- Sicurezza ed EMC (compatibilità elettromagnetica): nel caso di dispositivi attivi, i prototipi dovrebbero considerare, in anticipo, l'isolamento elettrico, la corrente di dispersione e altri indicatori di sicurezza per evitare, durante il funzionamento, di influenzare altre apparecchiature senza essere influenzati da interferenze esterne. La rettifica successiva viene pagata con un prezzo astronomicamente alto, e questa è una necessità da affrontare nella registrazione e nel test.
Incorporando i requisiti di conformità normativa nello sviluppo di prototipi di dispositivi medici è in realtà un approccio proattivo di gestione del rischio. Ciò eviterebbe drastiche modifiche progettuali dovute a problemi di funzionalità derivanti durante la registrazione, i test o la validazione clinica, risparmiando sostanzialmente molto tempo e denaro, e fungerebbe da pietra angolare per accelerare il lancio del prodotto .
In che modo la certificazione ISO 13485 influisce sul sistema di qualità per lo sviluppo di prototipi?
Prototipo ISO 13485 eleva il processo da un'attività potenzialmente casuale a un processo controllato, tracciabile e vitale che fornisce fiducia iniziale nella sicurezza e nell'efficacia del prodotto finale. Richiede un solido sistema di qualità fin dalla fase di ideazione in poi. Ciò si riflette in particolare in:
Rigorosi controlli di progettazione e gestione della documentazione
Per la prototipazione, è necessario disporre della documentazione di input, output, revisione e modifica della progettazione secondo lo standard ISO 13485. Sono necessarie specifiche completamente documentate, dalle specifiche dei requisiti del cliente ai record di revisione dei disegni e alle conclusioni della revisione del progetto. Ciò garantisce inoltre coerenza tra il prototipo e l'intento progettuale e costituisce un'utile "storia del progetto", fornendo prova diretta per le successive domande di registrazione.
Produzione Controllata e Tracciabilità
Questo standard richiede la verifica e il controllo dei processi chiave di prototipazione. Ad esempio, in termini di materiali di grado medico coinvolti, dovrebbero essere forniti certificati di qualificazione dei fornitori e registri di ispezione in entrata ; comporta anche l'impostazione e la conferma dei parametri delle apparecchiature di elaborazione, come lo spessore dello strato e la potenza del laser Stampa 3D . Ciò garantirebbe coerenza e ripetibilità in questo processo di prototipazione e fornire una base chiara per future repliche o iterazioni.
Integrazione anticipata della gestione del rischio
Le attività di gestione del rischio dovrebbero iniziare abbastanza presto durante la prototipazione per identificare i potenziali rischi associati alla progettazione, ai materiali e ai processi per i quali dovrebbero essere implementate misure di controllo. A tale riguardo, costringe il team a pensare in anticipo ai requisiti legati alla sicurezza, come la pulizia, la sterilizzazione e la biocompatibilità , e a integrare le soluzioni nella progettazione e produzione del prototipo , riducendo il rischio di importanti modifiche progettuali successive.
Il valore proveniente da a sistema di qualità durante l'intero processo di prototipazione va ben oltre il semplice ottenimento di un certificato ISO 13485 . Ciò produrrà, per il prototipo stesso, un quadro standardizzato e trasparente ; non solo un "campione" funzionale ma un " pre-prodotto " affidabile, completo di dati e con rischi controllati.
Selezione di materiali di grado medico che soddisfano i requisiti di biocompatibilità?
La selezione è il primo ostacolo nella determinazione della biocompatibilità e della sicurezza del prodotto nello sviluppo del prototipo del dispositivo medico . La selezione di un materiale appropriato riduce al minimo i rischi durante la registrazione ma, cosa più importante, garantisce la sicurezza del paziente. Per rendere più chiare le logiche di selezione, si confrontano di seguito le considerazioni chiave.
| Dimensioni di considerazione | Percorso Base: Selezione dei Materiali Certificati |
Percorso Avanzato: Valutazione Biologica dei Materiali |
| Principio | L'uso di materiali di grado medico con certificazione matura viene prima di tutto, come USP Classe VI o ISO 10993. | Se viene utilizzato un materiale innovativo, sarà necessaria una valutazione biologica completa secondo gli standard ISO 10993 . |
|
Scenari applicabili |
Si applica alla maggior parte dei materiali maturi a basso rischio e con un percorso chiaro e veloce. | Si applica a materiali nuovi e innovativi o a scenari di interazione uomo-uomo completamente nuovi con rischi e costi più elevati. |
| Prove chiave | Certificati di certificazione e rapporti di prova completamente compilati dal fornitore del materiale. |
Incaricare un laboratorio adeguatamente attrezzato e qualificato per eseguire la serie completa o parziale dei test di sicurezza richiesti. |
| Il nostro supporto | Forniamo abbinamenti rapidi e raccomandazioni basati su un database convalidato di materiali di grado medico , insieme a consulenza su schemi di valutazione e supporto per i test. | Supportiamo i clienti nel mitigare i rischi di conformità lungo l’intero processo. |
Consigliamo vivamente di pianificare la biocompatibilità fin dalle prime fasi della prototipazione, selezionando materiali precertificati da database validati per ridurre al minimo l'incertezza . Laddove si debbano coprire esigenze innovative, l’intero percorso di valutazione biologica sarà pianificato con molto anticipo. Ciò eviterebbe ritardi nella registrazione e interruzioni dei progetti dovuti a problemi materiali fin dall’inizio e getterebbe le basi per la sicurezza e il rapido lancio sul mercato dei prodotti.

Figura 2: Controllo volumetrico accurato per prototipi medici da LS Manufacturing
Quali standard dovrebbero soddisfare i prototipi nelle diverse fasi cliniche?
La maggior parte delle persone interpreta male prototipazione di dispositivi medici come un'attività in cui una versione di un prototipo cerca di soddisfare tutte le esigenze. Ciò spesso si traduce in uno spreco di risorse nell'utilizzo o nella mancanza di standard. Ciò che la scienza sostiene con precisione in ogni passaggio, dal concetto alla validazione clinica , è la realizzazione di prototipi "giusti", basati sugli obiettivi delle diverse fasi cliniche.
| Stadio clinico | Obiettivi fondamentali del prototipo | Standard e strategie di produzione |
| Prova di concetto | Verificare la fattibilità del concept progettuale nel più breve tempo possibile. | Metodi economici e rapidi, come la stampa 3D, possono raggiungere funzioni fondamentali. I materiali sono illimitati; ora è il momento di una rapida iterazione. |
| Test funzionali |
Condurre test ingegneristici completi sui prototipi. |
Convalida approfondita delle prestazioni e dell'affidabilità del prodotto utilizzando prototipi che rappresentano fedelmente le dimensioni, i materiali e le prestazioni del prodotto. |
| Test sugli animali | Il primo passo della procedura è valutare la sicurezza del prodotto in questione e la sua biocompatibilità . | Deve essere preparato da materiale biocompatibile di grado medico dopo il trattamento asettico in modo che i test siano validi. |
| Validazione clinica | I dati di sicurezza ed efficacia dovrebbero essere ottenuti da studi condotti sugli esseri umani. | Il prototipo deve essere rappresentativo del prodotto finale e deve essere conforme ad esso norme sui dispositivi medici rispetto a prestazioni, materiali e processi di produzione. |
In generale, la prototipazione di dispositivi medici funziona efficacemente con un approccio dinamico ma progressivo. Dalla fase di prova "economica" fino alla fase di "quasi-commercializzazione" , con validazione clinica , ciascuna fase della progettazione del prototipo dovrebbe fissare determinati obiettivi con standard corrispondenti. Tale strategia manterrà efficacemente sotto controllo i costi di ricerca e sviluppo nelle fasi iniziali, garantendo al tempo stesso l’ integrità e l’affidabilità della catena di dati del prototipo , evitando così ritardi o fallimenti del progetto a causa di standard di prototipo non corrispondenti.
Come si possono bilanciare precisione e producibilità nel prototipo degli strumenti chirurgici?
Nel processo di prototipo di strumenti chirurgici sviluppo, l'obiettivo è non solo ottenere una migliore precisione funzionale, ma anche dimostrare che il suo design può essere trasformato in modo stabile ed economico in prodotti qualificati prodotti in serie. Dovrebbe essere data priorità ai principi della progettazione finalizzata alla producibilità . Pertanto occorre tenere in considerazione i seguenti punti:
Semplificazione strutturale e ottimizzazione dell'assieme
Pur garantendo la funzionalità, il numero di parti dovrebbe essere ridotto al minimo ed evitare strutture interne complesse. Ad esempio, la tecnologia di stampa 3D integrata potrebbe essere utilizzata al posto delle tradizionali strutture di assemblaggio multiparte oppure potrebbero essere adottati design autobloccanti a scatto invece del fissaggio a vite. In tal modo, è possibile ridurre notevolmente le difficoltà e i tempi di assemblaggio successivo, migliorando quindi l’efficienza e la coerenza della produzione.
Abbinamento dei processi di produzione e progettazione delle tolleranze
Nella fase di prototipazione, dovrebbero essere considerati i processi coinvolti nella produzione di massa, come lo stampaggio a iniezione di precisione e Lavorazione a 5 assi e dovrebbero essere fissate tolleranze ragionevoli. Non è necessario perseguire la precisione estrema se le dimensioni di accoppiamento non sono critiche ; in caso contrario, il costo dell'elaborazione aumenterà notevolmente. I progettisti devono comprendere i limiti delle capacità dei diversi processi e lasciare margini ragionevoli per gli errori di produzione pur soddisfacendo i requisiti clinici.
Fattibilità della produzione in serie di materiali e trattamenti superficiali
La selezione dei materiali nel caso di un prototipo dovrebbe soddisfare non solo i requisiti di biocompatibilità e proprietà meccaniche, ma anche considerare la stabilità della catena di approvvigionamento e i costi nella produzione di massa. Nel frattempo, trattamenti superficiali speciali, come il rivestimento antibatterico, dovrebbero poter essere implementati in modo stabile e uniforme su lotti di parti piuttosto che su campioni di laboratorio.
Un prototipo di successo di uno strumento chirurgico incorpora considerazioni sulla producibilità fin dall'inizio. Identifica e ottimizza possibili problemi di produzione, qualità e costi per la produzione su larga scala . L'idea è quella di evitare di progettare un prodotto "perfetto" che sia improducibile o troppo costoso da realizzare, e anche di garantire che la transizione dal prototipo alla produzione di massa avvenga senza intoppi.
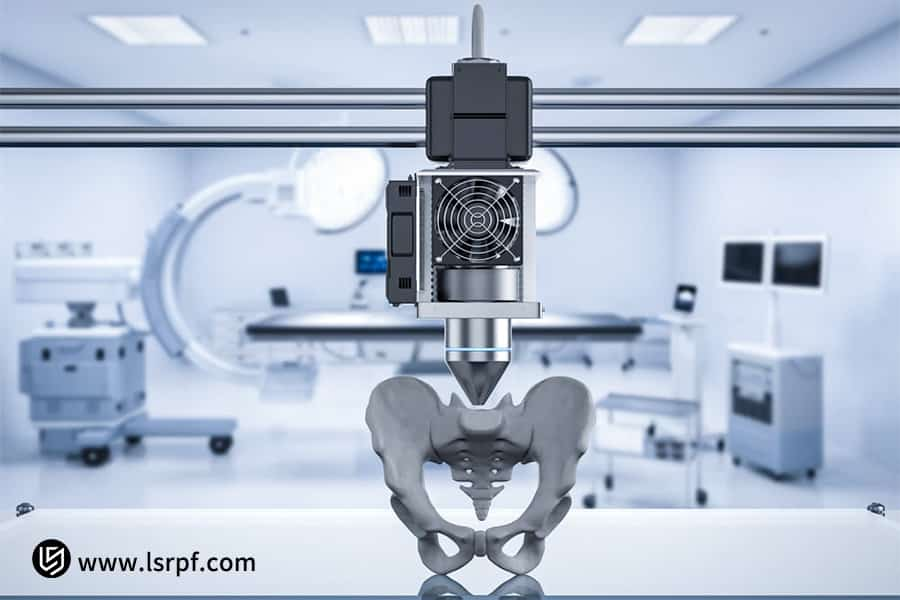
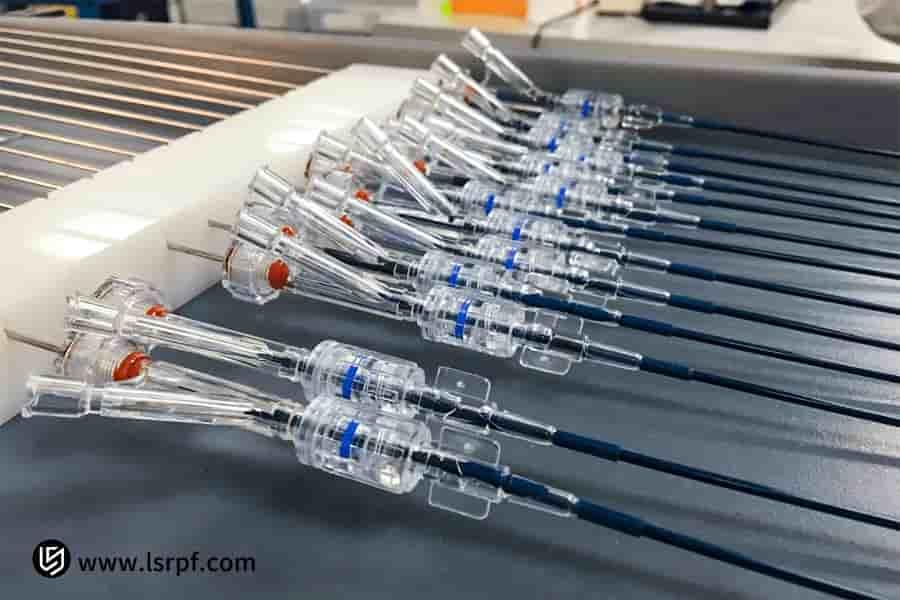
Figura 3: Sviluppo accelerato di impianti chirurgici su misura da parte di LS Manufacturing
In che modo la tecnologia di prototipazione rapida facilita l'innovazione nei dispositivi medici?
Il valore più importante di prototipazione rapida per dispositivi medici è che può abbreviare il periodo di tempo che intercorre tra la progettazione concettuale e la verifica fisica, fornendo una piattaforma molto efficace per tentativi ed errori e per l'iterazione. Tra queste tecnologie, la stampa 3D di grado medicale sta giocando un ruolo rivoluzionario, con i suoi vantaggi e requisiti che si riflettono in particolare in:
- Ottenimento di strutture complesse e personalizzazione personalizzata: microcanali complessi e strutture ossee trabecolari porose, difficili da elaborare con metodi tradizionali, possono essere facilmente prodotti con la stampa 3D di grado medico . È quindi possibile produrre guide chirurgiche e impianti personalizzati per conformarsi esattamente all'anatomia del paziente, uno sviluppo che contribuisce direttamente alla medicina di precisione.
- Integrazione di diversi materiali e funzioni: questi moderni tecnologie di prototipazione rapida consentono di produrre componenti a partire da una gamma di materiali che variano da rigidi e flessibili a biodegradabili, il tutto all'interno di un unico componente. Ad esempio, un componente integrato che combina una struttura rigida con una guarnizione morbida può essere stampato in un unico passaggio per essere utilizzato nei modelli anatomici che simulano organi reali o prototipi di dispositivi complessi per la somministrazione di farmaci.
- Soddisfare i requisiti particolari delle applicazioni mediche: la sicurezza e la conformità non possono mai essere sacrificate nella prototipazione rapida di dispositivi medici , non importa quanta velocità sia in gioco. I materiali devono essere biocompatibili e il processo di stampa stesso deve essere convalidato in modo tale da garantire la coerenza da lotto a lotto e la tracciabilità durante tutto il processo in base ai requisiti del sistema di qualità .
Si tratta di una classe di tecnologie di prototipazione rapida in cui stampa 3D di grado medico consente al team di ricerca e sviluppo di esplorare progetti precedentemente impossibili a un costo inferiore e in tempi record. Il controllo rigoroso su materiali e processi garantisce che l'innovazione segua il percorso di conformità fin dalla fase iniziale fino alla validazione clinica e alla registrazione del prodotto.
In che modo la produzione LS aiuta gli strumenti chirurgici mininvasivi a superare il collo di bottiglia tecnologico?
Il valore fondamentale nella ricerca e sviluppo dei dispositivi medici innovativi che offriamo è legato al suo servizi di prototipazione di dispositivi medici nell'aiutare i clienti a superare i principali colli di bottiglia tecnologici nel lancio dei loro prodotti. T L'illustrazione che segue è un caso tipico che dimostra l'applicazione del Prototipo medico di LS Manufacturing approccio:
Sfida del cliente
Nel processo di sviluppo di un nuovo tipo di strumento chirurgico minimamente invasivo , un dispositivo per anastomosi intracavitaria, un'azienda innovativa ha dovuto affrontare enormi ostacoli durante i test sugli animali. Il meccanismo di trasmissione centrale ha dimostrato un ritardo significativo nel funzionamento e non è stato in grado di fornire ai chirurghi un controllo efficace e preciso dell'azione dell'anastomosi. Limitato dal processo di produzione tradizionale, non c'era più spazio per ulteriori ottimizzazioni a causa della complicata struttura della trasmissione interna.
Soluzione di produzione LS
Intervenendo, il nostro team di ingegneri ha immediatamente abbandonato il metodo di lavorazione tradizionale. Abbiamo impiegato acciaio inossidabile di grado medico Tecnologia di stampa 3D , che produce un sistema di trasmissione in un solo passaggio e in un unico pezzo con un percorso meccanico superiore e un gioco estremamente minimo. Ciò non solo ha risolto il problema del ritardo; un ulteriore miglioramento è stato applicato all'elettrolucidatura di questa complessa cavità stampata in un unico pezzo , conferendole una finitura superficiale di gran lunga superiore a quella degli standard e soddisfacendo perfettamente gli elevatissimi requisiti di sterilità e pulizia degli strumenti chirurgici.
Risultati e valore
Nelle successive sperimentazioni sugli animali, il prototipo appena prodotto ha funzionato perfettamente e la velocità di risposta operativa e la precisione dello strumento sono migliorate di circa il 60% , ottenendo elogi da parte degli esperti clinici. Questa innovazione tecnologica ha quindi fatto avanzare direttamente il programma complessivo del progetto del cliente di almeno 5 mesi e ha consentito di risparmiare oltre 2 milioni di RMB in costi di ricerca e sviluppo sostenuti da ripetuti tentativi ed errori e dalla modifica dello stampo.
Abbiamo applicato tecnologie avanzate, come la stampa 3D di grado medico, per superare i limiti comuni di struttura, materiale e prestazioni strumenti chirurgici mini-invasivi per i nostri clienti Quelle che sembravano sfide tecniche impossibili sono diventate la chiave della competitività del prodotto, garantendo preziose finestre di time-to-market ed enormi vantaggi in termini di costi per i nostri clienti.

Figura 4: Dosaggio di precisione nella fabbricazione di prototipi medici da parte di LS Manufacturing
Che tipo di documentazione tecnica richiede lo sviluppo di prototipi nei dispositivi medici?
Pieno documentazione tecnica è la pietra angolare del successo della registrazione dei dispositivi medici. Serve principalmente a documentare in modo completo il processo di controllo della progettazione e a fornire prove sulla sicurezza e sull'efficacia del prodotto. Questa non costituirà solo una tabella di marcia per lo sviluppo interno, ma servirà anche come prova per le agenzie di regolamentazione della capacità di sviluppo sistematico e conforme dell'impresa. Comprenderà, ma non sarà limitato a, i seguenti documenti chiave:
- Documenti di input e output della progettazione: questo è l'inizio del sistema di documentazione: input di progettazione, che registreranno le esigenze degli utenti, le funzioni cliniche, gli indicatori di prestazione e gli standard normativi in modo chiaro. I risultati della progettazione includeranno disegni di prodotto, specifiche tecniche, elenchi di parti, ecc . Ogni input dovrebbe essere verificato per avere un output corrispondente.
- Certificazione dei materiali e documentazione sulla biocompatibilità: dovrebbero essere disponibili le certificazioni dei fornitori e i certificati dei materiali di tutti i materiali di grado medico, insieme alla valutazione della biocompatibilità o ai rapporti di test pertinenti alle parti di USP Classe VI o ISO 10993. Ciò è direttamente correlato alla determinazione della biocompatibilità del prodotto.
- Documenti di convalida del processo di produzione: dimostrare che il processo di produzione del prototipo è coerente e controllabile per ogni processo critico coinvolto nella sua creazione, come ad esempio Parametri di stampa 3D o processi di sterilizzazione , tramite registrazioni dettagliate dei parametri di processo, certificati di calibrazione delle apparecchiature e rapporti di ispezione del primo articolo.
In altre parole, significa che la creazione della documentazione tecnica è un'attività di base che corre parallela alla prototipazione e prepara l'avanzamento efficiente del progetto; non è un ripensamento. Un bene controllo della progettazione il sistema di documentazione, come il “certificato di nascita” del prodotto, mostra chiaramente il percorso progettuale dal concetto al prototipo.
Come pianificare il percorso della domanda di registrazione durante la fase di prototipazione?
Sulla base del valido lavoro di preparazione della domanda di registrazione , accelerare lo sviluppo di dispositivi medici può essere garantito e, in questo processo, ogni dato generato diventerà un valido supporto per i futuri documenti di registrazione. Vale a dire che dovrebbero essere sistematicamente pianificati i seguenti tre livelli:
Definire chiaramente i requisiti relativi alla prova della registrazione
La fase di input della progettazione del prototipo richiede l'analisi approfondita dei requisiti normativi del mercato di riferimento. I principali aspetti da verificare durante la revisione delle registrazioni, come gli indicatori di prestazione, la biocompatibilità e la sicurezza elettrica, vengono tradotti in parametri tecnici specifici che devono essere verificati dal prototipo. Ciò garantirebbe lo sviluppo di un prototipo sulla giusta strada conforme fin dall’inizio.
Trasformare i dati di validazione del prototipo in prove di registrazione
Il prototipo dovrà essere sottoposto a test funzionali, di durata e di usabilità conformi ai requisiti del sistema qualità . Tutti i test devono essere eseguiti con un protocollo standard pre-approvato, che dovrebbe includere una registrazione completa dei dati grezzi e un rapporto standardizzato. Si tratterà di dati altamente controllati che potranno poi essere presentati direttamente come prova fondamentale per la futura convalida della progettazione, evitando così di ripetere i test.
Stabilire un sistema trasparente per la documentazione della storia della progettazione
Dovrebbe fornire una registrazione completa del processo che va dall'input di progettazione alla revisione, alle modifiche e all'output. Questo sistema di documentazione formato naturalmente nel processo di controllo della progettazione può rivelarsi la prova migliore per dimostrare alle agenzie di regolamentazione che il processo di progettazione è rigoroso e controllato, il che può migliorare notevolmente l'efficienza e il tasso di successo delle revisioni della registrazione.
In altre parole, pianificazione domanda di registrazione l'integrazione nella fase di prototipo è la migliore leva per accelerare lo sviluppo di dispositivi medici , in quanto riduce notevolmente i costi elevati e i ritardi di tempo sostenuti nelle fasi successive del progetto a causa dei dati di registrazione supplementari, migliorando al contempo la standardizzazione e il tasso di successo dell'intero processo di ricerca e sviluppo fin dall'inizio, ponendo solide basi per un lancio sul mercato rapido e stabile dei prodotti
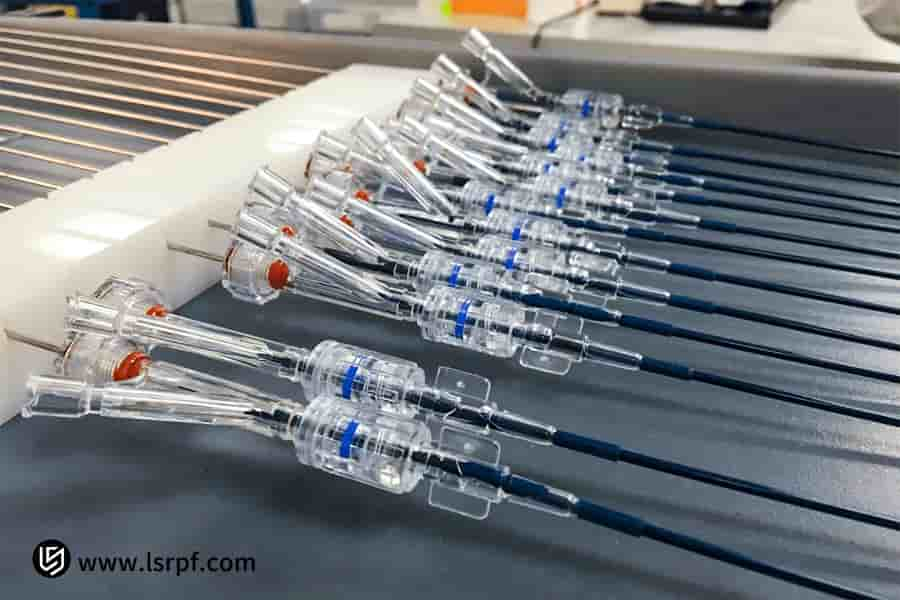
Figura 5: Prototipo a 360 gradi per la validazione funzionale da parte di LS Manufacturing
Domande frequenti
1. Quali requisiti specifici devono essere seguiti durante lo sviluppo di dispositivi medici prototipali?
Inoltre, oltre alla funzionalità di base, è necessario affrontare in modo proattivo il rispetto degli standard specifici per i dispositivi medici. Applichiamo rigorosamente il sistema di qualità ISO 13485 per garantire che questi prototipi soddisfino i requisiti normativi in materia di biocompatibilità, tolleranza alla sterilizzazione, sicurezza elettrica e altri aspetti fin dall'inizio della loro registrazione.
2. Quanto tempo passa dall'ideazione all'ottenimento del primo prototipo funzionale?
Dipende dalla complessità del dispositivo. I dispositivi relativamente semplici richiedono circa 2-3 settimane, mentre quelli più complessi con trasmissioni di precisione e componenti elettronici richiedono 4-6 settimane . Disponiamo di un canale rapido per affrontare in modo flessibile le esigenze urgenti di ricerca e sviluppo e garantire pienamente la pianificazione del progetto.
3. È possibile produrre piccoli lotti di dispositivi per sperimentazioni cliniche?
Naturalmente, uno dei nostri vari servizi è la fabbricazione di piccoli lotti di dispositivi per sperimentazioni cliniche , che vanno da 10 a 100 unità . La produzione era finita standard di produzione dei dispositivi medici e ogni unità sarà fabbricata secondo i più esigenti requisiti di prestazioni, qualità e coerenza per gli studi clinici.
4. Come garantite la biocompatibilità dei materiali del prototipo?
Controlliamo i rischi alla fonte attraverso la rigorosa selezione di materiali di grado medico con certificazioni autorevoli come ISO 10993 o USP Classe VI. Insieme al prototipo possono essere forniti documenti completi di certificazione del materiale, fornendo prove sostanziali per la valutazione della biocompatibilità.
5. Come proteggi la nostra proprietà intellettuale durante il processo di prototipazione?
La sicurezza delle informazioni è la nostra ancora di salvezza. Ogni progetto inizia con un accordo di riservatezza giuridicamente vincolante e internamente applichiamo un rigoroso sistema di gestione della gerarchia dei dati e di controllo degli accessi. Se richiesto dal cliente, possono essere realizzati anche firewall fisici e informativi.
6. Che tipo di prototipi di dispositivi medici supportate?
I servizi offerti dalla nostra azienda spaziano dai dispositivi attivi, come apparecchiature diagnostiche, a quelli passivi, compresi strumenti chirurgici, impianti e dispositivi non impiantabili . Produzione LS è esperto per quanto riguarda le normative e i processi associati ai vari prodotti.
7. Come rendere disponibili i dati del prototipo per l'utilizzo nelle domande di successiva registrazione?
Oltre ai prototipi, forniamo un pacchetto completo di prove di qualità, che comprende registrazioni dettagliate della produzione, rapporti di ispezione dei processi e dati sui test delle prestazioni . Tutti sono generati in base alle specifiche e possono essere direttamente utilizzati come materiale di verifica della progettazione per supportare le domande di registrazione.
8. Come avviare un progetto di prototipo di dispositivo medico?
Il processo per iniziare è piuttosto semplice: basta compilare alcuni schizzi concettuali iniziali o requisiti tecnici e faremo in modo che un ingegnere senior si colleghi con te entro un giorno lavorativo per discutere in modo approfondito le soluzioni tecniche e fornirti una valutazione iniziale del progetto e un preventivo.
Riepilogo
I prototipi di dispositivi medici sono molto più di una realizzazione tecnica; sono la pietra angolare della gestione del rischio, della conformità normativa e del successo commerciale. Trovare il giusto partner per la prototipazione pone solide basi per l’intero ciclo di vita del prodotto.
Pertanto, se vuoi accelerare la ricerca e sviluppo riducendo al contempo i rischi di registrazione, per favore contatta i nostri esperti nei dispositivi medici oggi per una "Soluzione di prototipazione orientata alla registrazione" per il tuo progetto! Applichiamo la nostra esperienza professionale nella produzione di dispositivi medici per proteggere il tuo percorso di innovazione.
📞Telefono: +86 185 6675 9667
📧E-mail: info@longshengmfg.com
🌐Sito web: https://lsrpf.com/
Disclaimer
Il contenuto di questa pagina è solo a scopo informativo. LS Manufacturing non rilascia dichiarazioni o garanzie, esplicite o implicite, in merito all'accuratezza, completezza o validità delle informazioni. Non si deve dedurre che fornitori o produttori di terze parti forniranno parametri prestazionali, tolleranze geometriche, caratteristiche di progettazione specifiche, qualità e tipo di materiali o processi attraverso la rete LS Manufacturing. L'acquirente è l'unico responsabile di queste informazioni. Per i preventivi delle parti, specificare i requisiti esatti per queste parti. Vi preghiamo di contattarci per ulteriori informazioni .
Squadra di produzione LS
LS Manufacturing è un'azienda leader del settore specializzata in soluzioni di produzione personalizzate. Con oltre 20 anni di esperienza al servizio di oltre 5.000 clienti, ci concentriamo sull'alta precisione Lavorazione CNC , fabbricazione di lamiere , Stampa 3D , stampaggio ad iniezione , stampaggio metalli e altri servizi di produzione one-stop.
La nostra fabbrica vanta oltre 100 centri di lavoro a cinque assi all'avanguardia ed è certificata ISO 9001:2015. Forniamo soluzioni di produzione rapide, efficienti e di alta qualità a clienti in oltre 150 paesi e regioni in tutto il mondo. Che si tratti di produzione in piccoli lotti o di personalizzazione di massa, possiamo soddisfare le vostre esigenze entro 24 ore. Scegliere LS Manufacturing significa scegliere efficienza, qualità e professionalità.
Per ulteriori informazioni, visitare il nostro sito Web: www.lsrpf.com .