Prototipo de dispositivo médico La misión principal de garantizar el cumplimiento normativo es fundamentalmente diferente de los prototipos de ingeniería general. En realidad, esta es la causa fundamental de los conceptos erróneos sobre la iteración lenta. En el modelo tradicional, separa la verificación funcional y regulatoria; por lo tanto, cuando se enfrentan desafíos regulatorios como la biocompatibilidad y la seguridad eléctrica, posteriormente se deben realizar modificaciones drásticas en el prototipo, lo que retrasa enormemente los ensayos clínicos y el registro.
La estrategia de " creación de prototipos orientada al registro " de LS Manufacturing incorpora los requisitos reglamentarios de manera sistemática desde la etapa de diseño. Coloca los estándares en la parte superior de su lista de prioridades para garantizar el cumplimiento de los elementos clave de registro junto con la realización funcional del prototipo, de modo que el prototipo esté calificado para la validación clínica y las pruebas de registro, asegurando así el éxito por primera vez en el lanzamiento del producto. Para ahorrarle tiempo, a continuación se ofrece una breve descripción general de los hallazgos clave.
Referencia rápida sobre creación de prototipos de dispositivos médicos
| Módulo | Conclusión clave |
| Concepto central | Crear " Prototipos Dirigidos a Registro " que incorporen función con cumplimiento normativo. |
| Puntos débiles tradicionales | La introducción de requisitos reglamentarios en una etapa tardía del proceso da como resultado modificaciones repetidas en el prototipo, lo que retrasa el tiempo de comercialización. |
| Elementos clave | La biocompatibilidad, la ingeniería de usabilidad y la gestión de riesgos se abordarán en conjunto en la fase de creación de prototipos. |
| Solución | Obtenga el diseño correcto a la primera mediante una supervisión regulatoria proactiva y trabajando en paralelo. |
| Valor final | Reducir drásticamente el riesgo de registro y acortar sustancialmente el ciclo total de lanzamiento del producto. |
La siguiente tabla ilustra cómo acelerar el desarrollo de dispositivos médicos . cambiando los requisitos regulatorios desde "obstáculos en la última etapa" hasta "aportes de diseño en las primeras etapas". El movimiento hacia un enfoque "orientado al registro" significa que el prototipo mismo se convertirá en la base del registro, sin modificaciones posteriores perturbadoras, con el objetivo de un lanzamiento al mercado eficiente, confiable y rápido.
¿Por qué confiar en esta guía? Experiencia práctica de los expertos en fabricación de LS
Hay varios miles de artículos en línea sobre el tema de la creación de prototipos de dispositivos médicos, entonces, ¿por qué debería dedicar su tiempo a leer este? Lo que compartimos aquí no proviene de una definición de libro de texto, sino más bien de algunas pautas prácticas sujetas a las rigurosas limitaciones de la norma ISO 13485 y ISO9001 sistema y validado a través de innumerables cirugías y resultados de pruebas.
Durante más de una década, nuestro equipo ha fabricado más de 50.000 prototipos personalizados que cumplen con los ISO 13485 para dispositivos médicos requisitos del sistema de calidad. Cada proyecto nos brindó una comprensión más profunda de cómo establecer los parámetros de corte para aleaciones de magnesio biodegradables sin daño térmico, cómo mantener la estabilidad en estructuras de paredes delgadas durante el microfresado y cómo implementar simultáneamente los requisitos de gestión de riesgos e ingeniería de usabilidad en cada paso de la iteración.
Créanos, lo que lee aquí es la metodología central que utilizamos a diario para superar los desafíos. Trabajemos juntos para transformar sus ideas novedosas con eficiencia y confiabilidad en productos confiables.

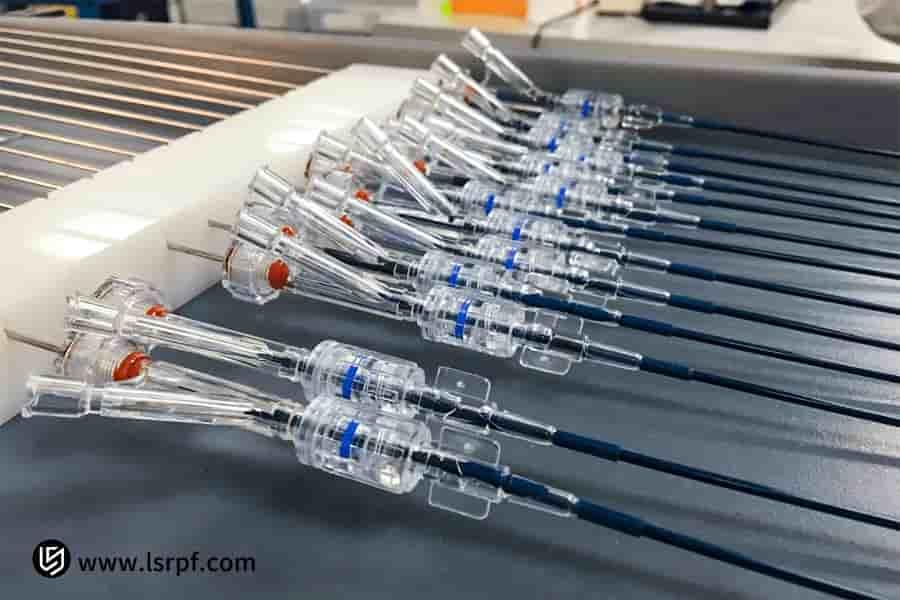
Figura 1: Prototipo integral para verificación de funcionalidad por parte de LS Manufacturing
¿Por qué los prototipos de dispositivos médicos deberían ir más allá de la "validación funcional"?
El objetivo final del prototipo de dispositivo médico no es sólo ser un modelo "funcional", sino un " prototipo de producto " que sea capaz de superar todos los rigurosos procesos de registro y aprobación y aplicarse de forma segura en el cuerpo humano. Por tanto, el alcance de su validación debe incluir el ciclo de vida completo de los riesgos de uso.
- Tolerancia a la esterilidad: un prototipo puede tener una función motora perfecta pero no soportar procesos de esterilización repetidos, como altas temperaturas y presiones, irradiación o inmersión química . El envejecimiento del material puede degradar su rendimiento y causar infección clínica. Los materiales compatibles deben seleccionarse y validarse durante la etapa de prototipo .
- Descripción general de la biocompatibilidad: Las piezas que entren en contacto directo o indirecto con los pacientes deben estar fabricadas con materiales no tóxicos y no alérgicos . Este reemplazo por materiales biocompatibles más adelante en el proceso de diseño puede afectar sus propiedades mecánicas y requerir un rediseño estructural completo.
- Seguridad y EMC (Compatibilidad Electromagnética): En el caso de dispositivos activos, los prototipos deben considerar previamente el aislamiento eléctrico, la corriente de fuga y otros indicadores de seguridad para evitar, durante la operación, influir en otros equipos sin ser influenciados por interferencias externas. La rectificación posterior se paga con un precio astronómicamente alto, y esa es una necesidad que hay que afrontar en el registro y las pruebas.
Incorporar los requisitos de cumplimiento normativo El desarrollo de prototipos de dispositivos médicos es en realidad un enfoque proactivo de gestión de riesgos. Esto evitaría cambios drásticos en el diseño debido a problemas de funcionalidad que surgen durante el registro y las pruebas o la validación clínica (lo que fundamentalmente ahorraría mucho tiempo y dinero) y actuaría como piedra angular para acelerar el lanzamiento del producto .
¿Cómo afecta la certificación ISO 13485 al sistema de calidad para el desarrollo de prototipos?
Prototipo ISO 13485 eleva el proceso de una actividad potencialmente azarosa a un proceso controlado, rastreable y vital que proporciona confianza temprana en la seguridad y eficacia del producto final. Requiere un sistema de calidad sólido desde la etapa de concepto en adelante. Esto se refleja particularmente en:
Estrictos controles de diseño y gestión de la documentación
Para la creación de prototipos, se requiere contar con documentación de entrada, salida, revisión y cambio del diseño de acuerdo con la norma ISO 13485. Se requieren especificaciones completamente documentadas, desde las especificaciones de los requisitos del cliente hasta los registros de revisión de los planos y las conclusiones de la revisión del diseño. Esto también proporciona coherencia entre el prototipo y la intención del diseño y forma un "historial de diseño" útil, que proporciona evidencia directa para solicitudes de registro posteriores.
Fabricación Controlada y Trazabilidad
Este estándar requiere verificación y control de procesos clave de creación de prototipos. Por ejemplo, en términos de los materiales de grado médico involucrados, se deben proporcionar certificados de calificación del proveedor y registros de inspección entrantes ; También implica la configuración y confirmación de los parámetros del equipo de procesamiento, como el espesor de la capa y la potencia del láser en impresión 3D . Esto aseguraría coherencia y repetibilidad en este proceso de creación de prototipos y proporciona una base clara para futuras replicaciones o iteraciones.
Integración temprana de la gestión de riesgos
Las actividades de gestión de riesgos deben comenzar lo suficientemente temprano durante la creación de prototipos para identificar los riesgos potenciales asociados con el diseño, los materiales y los procesos para los cuales se deben implementar medidas de control. En ese sentido, obliga al equipo a pensar de antemano en los requisitos relacionados con la seguridad, como la limpieza, la esterilización y la biocompatibilidad , e integrar las soluciones en el diseño y la fabricación del prototipo , reduciendo la posibilidad de cambios importantes de diseño posteriores.
El valor proveniente de un sistema de calidad a lo largo de todo el proceso de creación de prototipos va mucho más allá de la simple obtención de un certificado en ISO 13485 . Esto producirá, para el propio prototipo, un marco estandarizado y transparente ; no sólo una "muestra" funcional sino un " preproducto " confiable, con datos completos y con riesgos controlados.
¿Selección de materiales de grado médico que cumplan con los requisitos de biocompatibilidad?
La selección es el primer obstáculo en la determinación de la biocompatibilidad y seguridad del producto en el desarrollo del prototipo de dispositivo médico . La selección de un material adecuado minimiza los riesgos en el registro pero, lo más importante, garantiza la seguridad del paciente. Para aclarar la lógica de selección, las consideraciones clave se comparan a continuación.
| Dimensiones de consideración | Camino Básico: Selección de Materiales Certificados |
Ruta Avanzada: Evaluación Biológica de Materiales |
| Principio | el uso de materiales de grado medico con una certificación madura es lo primero, como USP Clase VI o ISO 10993. | Si se utiliza un material innovador, se requerirá una evaluación biológica completa bajo las normas ISO 10993 . |
|
Escenarios aplicables |
Aplica para la mayoría de materiales maduros, de bajo riesgo y que tengan un recorrido claro y rápido. | Se aplica a materiales nuevos e innovadores o escenarios de interacción humano-humano completamente nuevos de mayor riesgo y costo. |
| Evidencia clave | Certificados de certificación e informes de prueba completamente completos del proveedor del material. |
Puesta en servicio de un laboratorio debidamente equipado y cualificado para realizar el conjunto total o parcial de pruebas de seguridad requeridas. |
| Nuestro apoyo | Proporcionamos coincidencias rápidas y recomendaciones basadas en una base de datos validada de materiales de grado médico , junto con consultas sobre esquemas de evaluación y soporte para pruebas. | Apoyamos a los clientes en la mitigación de los riesgos de cumplimiento a lo largo de todo el proceso. |
Recomendamos encarecidamente planificar la biocompatibilidad desde las primeras etapas de creación de prototipos, seleccionando materiales precertificados de bases de datos validadas para minimizar la incertidumbre . Cuando se deban cubrir necesidades innovadoras, el camino completo de la evaluación biológica se planificará con mucha antelación. Esto evitaría retrasos en el registro y perturbaciones en los diseños debido a problemas materiales desde el principio y sentaría las bases para la seguridad y el rápido lanzamiento al mercado de los productos.

Figura 2: Control volumétrico preciso para prototipos médicos de LS Manufacturing
¿Qué estándares deben cumplir los prototipos en diferentes etapas clínicas?
La mayoría de la gente malinterpreta creación de prototipos de dispositivos médicos como una actividad en la que una versión de un prototipo intenta satisfacer todas las necesidades. Esto a menudo resulta en el desperdicio de recursos en el uso o en la falta de estándares. Lo que la ciencia respalda precisamente en cada paso, desde el concepto hasta la validación clínica , es la elaboración de prototipos "perfectos", basados en los objetivos de las diferentes etapas clínicas.
| Etapa clínica | Objetivos centrales del prototipo | Estándares y estrategias de producción |
| Prueba de concepto | Verificar la viabilidad del concepto de diseño lo antes posible. | Los métodos económicos y rápidos, como la impresión 3D, pueden lograr funciones básicas. Los materiales son ilimitados; ahora es el momento de una iteración rápida. |
| Pruebas funcionales |
Realizar pruebas integrales de ingeniería de prototipos. |
Validación exhaustiva del rendimiento y la confiabilidad del producto utilizando prototipos que son representaciones cercanas del tamaño, los materiales y el rendimiento del producto. |
| Experimentación con animales | El primer paso del procedimiento es evaluar la seguridad del producto en cuestión y su biocompatibilidad . | Debe prepararse a partir de material biocompatible de grado médico tras un procesamiento aséptico para que las pruebas sean válidas. |
| Validación clínica | Los datos de seguridad y eficacia deben obtenerse en ensayos realizados en humanos. | El prototipo debe ser representativo del producto final y debe ajustarse a normas de dispositivos médicos con respecto al rendimiento, materiales y procesos de fabricación. |
En términos generales, la creación de prototipos de dispositivos médicos funciona eficazmente con un enfoque dinámico pero progresivo. Desde la etapa de prueba de concepto "económica" hasta la etapa de "cuasi-comercialización" , con validación clínica , cada etapa del diseño del prototipo debe establecer ciertos objetivos con estándares coincidentes. Una estrategia de este tipo mantendrá bajo control los costos de I+D en las primeras etapas y, al mismo tiempo, garantizará la integridad y confiabilidad de la cadena de datos del prototipo , evitando así retrasos o fallas en el proyecto debido a estándares de prototipo no coincidentes.
¿Cómo se pueden equilibrar la precisión y la capacidad de fabricación en el prototipo de instrumentos quirúrgicos?
En vías de prototipo de instrumentos quirúrgicos desarrollo, el objetivo no sólo es lograr una mejor precisión funcional sino también demostrar que su diseño se puede transformar de manera estable y económica en productos calificados producidos en masa. Se debe prestar atención prioritaria a los principios de diseño para la capacidad de fabricación . Por lo tanto, se deben tener en cuenta los siguientes puntos:
Simplificación estructural y optimización del montaje
Al tiempo que se garantiza la funcionalidad, se debe minimizar el número de piezas y evitar estructuras internas complejas. Por ejemplo, se podría utilizar tecnología de impresión 3D integrada en lugar de las estructuras de ensamblaje tradicionales de varias partes o se podrían adoptar diseños de ajuste a presión con cierre automático en lugar de fijación con tornillos. Al hacerlo, se pueden reducir considerablemente la dificultad y el tiempo de montaje posterior, mejorando así la eficiencia y la coherencia de la producción.
Coincidencia de procesos de fabricación y diseño de tolerancias
En la etapa de creación de prototipos se deben considerar los procesos involucrados en la producción en masa, como el moldeo por inyección de precisión y Mecanizado de 5 ejes , y se deben establecer tolerancias razonables. No es necesario buscar una precisión extrema si las dimensiones de acoplamiento no son críticas ; de lo contrario, el coste de procesamiento aumentará considerablemente. Los diseñadores deben comprender los límites de capacidad de los diferentes procesos y dejar márgenes razonables para errores de fabricación mientras cumplen con los requisitos clínicos.
Viabilidad de la producción en masa de materiales y tratamientos superficiales.
La selección del material en el caso de un prototipo debe cumplir no sólo los requisitos de biocompatibilidad y propiedades mecánicas, sino también considerar la estabilidad de la cadena de suministro y el costo de la producción en masa. Mientras tanto, los tratamientos superficiales especiales, como el recubrimiento antibacteriano, deberían poder implementarse de manera estable y uniforme en lotes de piezas en lugar de muestras de laboratorio.
Un prototipo exitoso de un instrumento quirúrgico incorpora consideraciones de fabricación desde el principio. Identifica y optimiza posibles problemas de fabricación, calidad y costos para la producción a gran escala . La idea es evitar diseñar un producto "perfecto" que sea improducible o demasiado caro de fabricar, y también garantizar que la transición del prototipo a la producción en masa sea fluida.
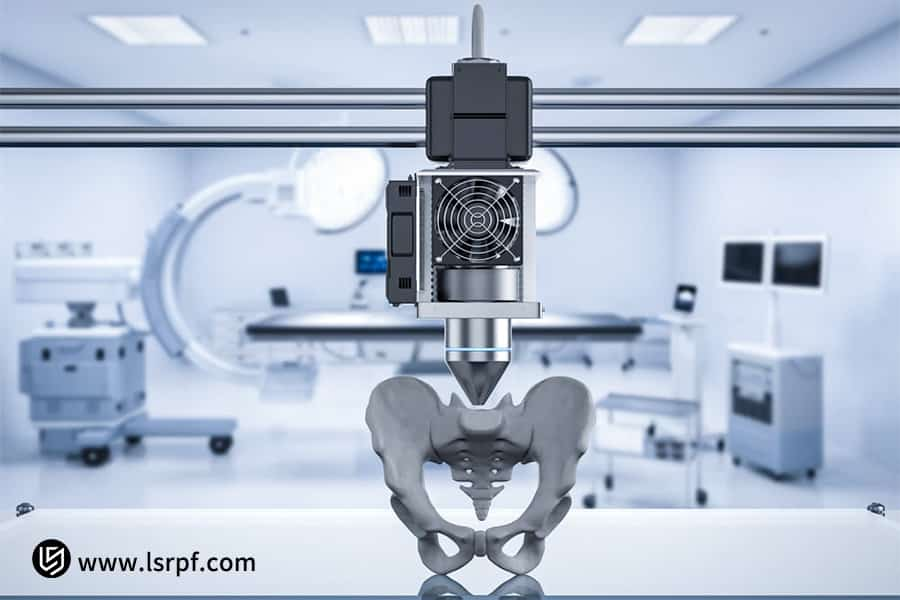
Figura 3: Desarrollo acelerado de implantes quirúrgicos personalizados por parte de LS Manufacturing
¿Cómo facilita la tecnología de creación rápida de prototipos la innovación en dispositivos médicos?
El valor más importante de creación rápida de prototipos para dispositivos médicos es que puede acortar el período de tiempo desde el diseño conceptual hasta la verificación física, proporcionando una plataforma muy efectiva para prueba, error e iteración. Entre estas tecnologías, la impresión 3D de grado médico está desempeñando un papel revolucionario, con sus ventajas y requisitos reflejados particularmente en:
- Lograr estructuras complejas y personalización personalizada: microcanales complejos y estructuras óseas trabeculares porosas, difíciles de procesar con métodos tradicionales, se pueden producir fácilmente con impresión 3D de grado médico . Por lo tanto, se pueden fabricar guías quirúrgicas e implantes personalizados para adaptarse exactamente a la anatomía del paciente, un desarrollo que contribuye directamente a la medicina de precisión.
- Integración de varios materiales y funciones: estos modernos tecnologías de creación rápida de prototipos permiten fabricar componentes a partir de una variedad de materiales que varían desde rígidos y flexibles hasta biodegradables, todo dentro de un solo componente. Por ejemplo, un componente integrado que combina una estructura rígida con un sello blando se puede imprimir en un solo paso para su uso en modelos anatómicos que simulan órganos reales o prototipos de dispositivos complejos de administración de fármacos.
- Cumplir con los requisitos particulares de las aplicaciones médicas: la seguridad y el cumplimiento nunca pueden sacrificarse en la creación rápida de prototipos para dispositivos médicos , sin importar cuánta velocidad esté en juego. Los materiales deben ser biocompatibles y el proceso de impresión en sí debe validarse de tal manera que garantice la coherencia entre lotes y la trazabilidad durante todo el proceso de acuerdo con los requisitos del sistema de calidad .
Se trata de una clase de tecnologías de creación rápida de prototipos en las que impresión 3D de grado médico permite al equipo de I+D explorar diseños que antes eran imposibles a un coste menor y en un tiempo récord. El riguroso control de los materiales y los procesos garantiza que la innovación siga el camino del cumplimiento desde la etapa inicial hasta la validación clínica y el registro del producto.
¿Cómo ayuda LS Manufacturing a los instrumentos quirúrgicos mínimamente invasivos a superar el cuello de botella tecnológico?
El valor central en la I+D de dispositivos médicos innovadores que ofrecemos se relaciona con su servicios de creación de prototipos de dispositivos médicos para ayudar a los clientes a superar los principales obstáculos tecnológicos en el lanzamiento de sus productos. t La siguiente es una ilustración de caso típico que demuestra la aplicación de la Prototipo médico de LS Manufacturing acercarse:
Desafío del cliente
En el proceso de desarrollo de un nuevo tipo de instrumento quirúrgico mínimamente invasivo , un dispositivo de anastomosis intracavitaria, una empresa innovadora se topó con enormes obstáculos durante las pruebas con animales. El mecanismo de transmisión central demostró un retraso significativo en su funcionamiento y no pudo proporcionar a los cirujanos un control eficaz y preciso de la acción de la anastomosis. Restringido por el proceso de fabricación tradicional, no había lugar para una mayor optimización debido a su complicada estructura de transmisión interna.
Solución de fabricación LS
Al intervenir, nuestro equipo de ingeniería abandonó inmediatamente el método de mecanizado tradicional. nosotros empleamos acero inoxidable de grado médico Tecnología de impresión 3D , que fabrica un sistema de transmisión de un solo paso y de una sola pieza con una trayectoria mecánica superior y un espacio mínimo extremo. Esto no sólo resolvió el problema del retraso; Para mejorar aún más, se aplicó electropulido a esta compleja cavidad moldeada de una sola pieza , dándole un acabado superficial muy superior al de los estándares y cumpliendo perfectamente con los extremadamente altos requisitos de esterilidad y limpieza de los instrumentos quirúrgicos.
Resultados y valor
En ensayos posteriores con animales, el prototipo recién fabricado funcionó perfectamente y la velocidad de respuesta operativa y la precisión del instrumento mejoraron en aproximadamente un 60% , lo que le valió grandes elogios por parte de los expertos clínicos. Por lo tanto, este avance tecnológico avanzó directamente el cronograma general del proyecto del cliente en al menos 5 meses y ahorró más de 2 millones de RMB en costos de I+D incurridos por pruebas y errores repetidos y modificaciones de moldes.
Aplicamos tecnologías avanzadas, como la impresión 3D de grado médico, para superar las limitaciones comunes de estructura, material y rendimiento de instrumentos quirúrgicos mínimamente invasivos para nuestros clientes. Lo que parecían desafíos técnicos imposibles se convirtieron en la competitividad clave del producto, asegurando valiosos plazos de comercialización y enormes ventajas de costos para nuestros clientes.

Figura 4: Dosificación de precisión en la fabricación de prototipos médicos por LS Manufacturing
¿Qué tipo de documentación técnica requiere el desarrollo de prototipos en dispositivos médicos?
Lleno documentación técnica es la piedra angular del registro exitoso de un dispositivo médico. Sirve principalmente para documentar exhaustivamente el proceso de control del diseño y proporcionar evidencia sobre la seguridad y eficacia del producto. Esto no sólo será una hoja de ruta para el desarrollo interno, sino que también servirá como evidencia para las agencias reguladoras de la capacidad de desarrollo sistemático y compatible de la empresa. Incluirá, entre otros, los siguientes documentos clave:
- Diseñar documentos de entrada y salida: Este es el comienzo del sistema de documentación: diseñar entradas, que registrarán las necesidades del usuario, las funciones clínicas, los indicadores de desempeño y los estándares regulatorios de manera clara. Los resultados del diseño incluirán dibujos de productos, especificaciones técnicas, listas de piezas, etc. Se debe verificar que cada entrada tenga una salida correspondiente.
- Certificación de materiales y documentación de biocompatibilidad: Deben estar disponibles las certificaciones de proveedores y los certificados de materiales de todos los materiales de grado médico, junto con evaluaciones de biocompatibilidad o informes de pruebas relevantes para partes de USP Clase VI o ISO 10993. Esto se relaciona directamente con el establecimiento de la biocompatibilidad del producto.
- Registros de validación del proceso de fabricación: demostrar que el proceso de fabricación del prototipo es consistente y controlable para cada proceso crítico involucrado en su creación, como Parámetros de impresión 3D o procesos de esterilización , a través de registros detallados de parámetros de proceso, certificados de calibración de equipos e informes de inspección del primer artículo.
En otras palabras, significa que la creación de documentación técnica como actividad básica que corre paralela a la creación de prototipos prepara para el progreso eficiente del proyecto; no es una ocurrencia tardía. un buen control de diseño El sistema de documentación, como el "certificado de nacimiento" del producto, muestra claramente la trayectoria del diseño desde el concepto hasta el prototipo.
¿Cómo planificar la ruta de solicitud de registro durante la etapa de creación de prototipos?
Basado en el sólido trabajo de preparación de la solicitud de registro , acelerar el desarrollo de dispositivos médicos puede estar seguro, y en este proceso, cada dato generado se convertirá en un fuerte soporte para futuros documentos de registro. Es decir, se deben planificar sistemáticamente los siguientes tres niveles:
Definir claramente los requisitos relativos a la prueba de registro
La fase de entrada del diseño del prototipo exige un análisis en profundidad de los requisitos reglamentarios del mercado objetivo. Los principales aspectos que deben comprobarse durante la revisión de las matriculaciones, como los indicadores de rendimiento, la biocompatibilidad y la seguridad eléctrica, se traducen en parámetros técnicos específicos que el prototipo debe verificar. Esto garantizaría el desarrollo de un prototipo en el camino correcto desde el principio.
Transforme los datos de validación del prototipo en evidencia de registro.
El prototipo deberá someterse a pruebas de funcionalidad, vida útil y usabilidad que cumplan con los requisitos del sistema de calidad . Todas las pruebas deben realizarse con un protocolo estándar previamente aprobado, que debe incluir un registro completo de datos sin procesar y un informe estandarizado. Serán datos altamente controlados que luego podrán presentarse directamente como evidencia central para la futura validación del diseño, evitando así la repetición de pruebas.
Establecer un sistema transparente para la documentación del historial del diseño.
Debe proporcionar un registro completo del proceso que fluye desde la entrada del diseño hasta la revisión, los cambios y la salida. Este sistema de documentación formado naturalmente en el proceso de control del diseño puede resultar la mejor evidencia para demostrar a las agencias reguladoras que el proceso de diseño es riguroso y controlado, lo que puede mejorar en gran medida la eficiencia y la tasa de éxito de las revisiones de registro.
En otras palabras, planificar solicitud de registro La integración en la fase de prototipo es la mejor palanca para acelerar el desarrollo de dispositivos médicos , ya que reduce en gran medida los altos costos y los retrasos en las fases posteriores del proyecto debido a los datos de registro complementarios, al tiempo que mejora la estandarización y la tasa de éxito de todo el proceso de I+D desde el principio, sentando una base sólida para un lanzamiento rápido y estable de los productos al mercado.
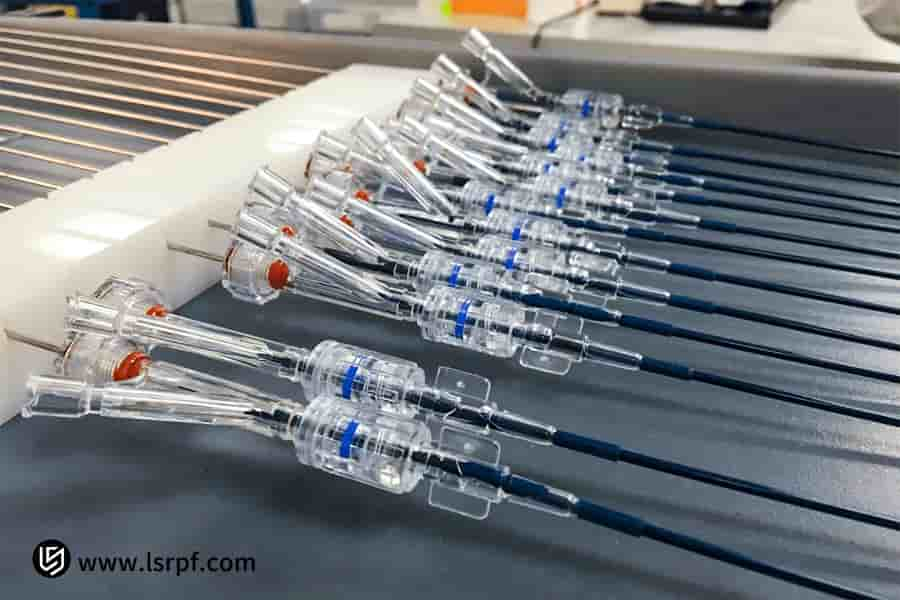
Figura 5: Prototipo de 360 grados para validación funcional por parte de LS Manufacturing
Preguntas frecuentes
1. ¿Qué requisitos específicos se deben seguir durante el desarrollo de prototipos de dispositivos médicos?
Además, más allá de la funcionalidad básica, es necesario abordar de manera proactiva el cumplimiento de los estándares particulares para dispositivos médicos. Aplicamos rigurosamente el sistema de calidad de ISO 13485 para garantizar que estos prototipos cumplan con los requisitos reglamentarios en biocompatibilidad, tolerancia a la esterilización, seguridad eléctrica y otros aspectos desde el inicio de su registro.
2. ¿Cuánto tiempo pasa desde el concepto hasta la obtención del primer prototipo funcional?
Depende de la complejidad del dispositivo. Los dispositivos relativamente simples tardan entre 2 y 3 semanas, mientras que los más complejos con transmisiones de precisión y componentes electrónicos tardan entre 4 y 6 semanas . Contamos con un canal acelerado para abordar de manera flexible las necesidades urgentes de I+D y garantizar plenamente el cronograma de su proyecto.
3. ¿Es posible fabricar pequeños lotes de dispositivos para ensayos clínicos?
Por supuesto, uno de nuestros diversos servicios es la fabricación de pequeños lotes de dispositivos para ensayos clínicos , que van desde 10 a 100 unidades . La fabricación fue por estándares de fabricación de dispositivos médicos , y cada unidad se fabricará con el rendimiento, la calidad y la coherencia exigentes para los ensayos clínicos.
4. ¿Cómo se garantiza la biocompatibilidad de los materiales prototipo?
Controlamos los riesgos desde la fuente mediante la estricta selección de materiales de grado médico con certificaciones autorizadas como ISO 10993 o USP Clase VI. Se pueden proporcionar documentos completos de certificación del material junto con el prototipo, lo que proporciona evidencia sustancial para su evaluación de biocompatibilidad.
5. ¿Cómo se protege nuestra propiedad intelectual durante el proceso de creación de prototipos?
La seguridad de la información es nuestro salvavidas. Cada proyecto comienza con un acuerdo de confidencialidad legalmente vinculante e internamente aplicamos un estricto sistema de gestión de jerarquía de datos y control de acceso. Si lo solicita el cliente, también se podrán establecer cortafuegos físicos y de información.
6. ¿Qué tipo de prototipos de dispositivos médicos apoyan?
Los servicios que ofrece nuestra empresa van desde dispositivos activos, como equipos de diagnóstico, hasta pasivos, incluyendo instrumentos quirúrgicos, implantes y dispositivos no implantables . Fabricación LS está bien versado en las regulaciones y procesos asociados con diversos productos.
7. ¿Cómo hacer que los datos del prototipo estén disponibles para su uso en solicitudes de registro posterior?
Además de los prototipos, proporcionamos un paquete completo de pruebas de calidad, que incluye registros de producción detallados, informes de inspección de procesos y datos de pruebas de rendimiento . Todos se generan según especificaciones y pueden utilizarse directamente como material de verificación de diseño para respaldar las solicitudes de registro.
8. ¿Cómo iniciar un proyecto de prototipo de dispositivo médico?
El proceso para comenzar es bastante simple: simplemente complete algunos bocetos conceptuales iniciales o requisitos técnicos, y nos aseguraremos de que un ingeniero senior se comunique con usted dentro de un día hábil para discutir las soluciones técnicas en profundidad y brindarle una evaluación y cotización inicial del proyecto.
Resumen
Los prototipos de dispositivos médicos son mucho más que una realización técnica; son la piedra angular de la gestión de riesgos, el cumplimiento normativo y el éxito comercial. Encontrar el socio adecuado para la creación de prototipos sienta una base sólida para todo el ciclo de vida del producto.
Por lo tanto, si desea acelerar la I+D y al mismo tiempo reducir los riesgos de registro, por favor contacta con nuestros expertos en dispositivos médicos hoy para una "solución de creación de prototipos orientada al registro" para su proyecto. Apliquemos nuestra experiencia profesional en la fabricación de dispositivos médicos para proteger su viaje de innovación.
📞Teléfono: +86 185 6675 9667
📧Correo electrónico: info@longshengmfg.com
🌐Sitio web: https://lsrpf.com/
Descargo de responsabilidad
El contenido de esta página es sólo para fines informativos. LS Manufacturing no ofrece ninguna representación ni garantía, expresa o implícita, con respecto a la exactitud, integridad o validez de la información. No se debe inferir que los proveedores o fabricantes externos proporcionarán parámetros de rendimiento, tolerancias geométricas, características de diseño específicas, calidad y tipo de material o procesos a través de la red de LS Manufacturing. El comprador es el único responsable de esta información. Para cotizaciones de piezas, especifique los requisitos exactos para estas piezas. Por favor contáctenos para más información .
Equipo de fabricación de LS
LS Manufacturing es una empresa líder en la industria especializada en soluciones de fabricación personalizadas. Con más de 20 años de experiencia sirviendo a más de 5000 clientes, nos enfocamos en alta precisión. Mecanizado CNC , fabricación de chapa , impresión 3D , moldeo por inyección , estampado de metales y otros servicios de fabricación integrales.
Nuestra fábrica cuenta con más de 100 centros de mecanizado de cinco ejes de última generación y cuenta con la certificación ISO 9001:2015. Brindamos soluciones de fabricación rápidas, eficientes y de alta calidad a clientes en más de 150 países y regiones de todo el mundo. Ya sea que se trate de producción en lotes pequeños o personalización en masa, podemos satisfacer sus necesidades en 24 horas. Elegir LS Manufacturing significa elegir eficiencia, calidad y profesionalidad.
Para obtener más información, visite nuestro sitio web: www.lsrpf.com .