Protótipo de dispositivo médico A missão principal de garantir a conformidade regulatória é fundamentalmente diferente dos protótipos de engenharia em geral. Na verdade, esta é a causa raiz dos equívocos sobre a iteração lenta. No modelo tradicional, separa a verificação funcional da regulatória; assim, ao enfrentar desafios regulamentares como a biocompatibilidade e a segurança eléctrica, mais tarde terão de ser feitas modificações drásticas no protótipo, atrasando enormemente os ensaios clínicos e o registo.
A estratégia de “ Prototipagem Orientada ao Registo ” da LS Manufacturing incorpora os requisitos regulamentares de forma sistemática desde a fase de concepção. Coloca as normas no topo da sua lista de prioridades para garantir o cumprimento dos principais elementos de registo em conjunto com a realização funcional do protótipo, de modo que o protótipo seja qualificado para validação clínica e testes de registo, garantindo assim o sucesso inicial no lançamento do produto. Para economizar seu tempo, aqui está uma breve visão geral das principais descobertas.
Referência rápida sobre prototipagem de dispositivos médicos
| Módulo | Principal vantagem |
| Conceito Central | Crie " Protótipos Dirigidos por Registro " que incorporem função com conformidade regulatória. |
| Pontos de dor tradicionais | A introdução de requisitos regulamentares numa fase tardia do processo resulta em modificações repetidas no protótipo, atrasando o tempo de colocação no mercado. |
| Elementos-chave | Biocompatibilidade, engenharia de usabilidade e gerenciamento de risco devem ser abordados em conjunto na fase de prototipagem. |
| Solução | Acerte o projeto na primeira tentativa por meio de supervisão regulatória proativa e trabalhando em paralelo. |
| Valor final | Reduzindo drasticamente o risco de registro e encurtando substancialmente o ciclo total de lançamento do produto. |
A tabela a seguir ilustra como acelerar o desenvolvimento de dispositivos médicos mudando os requisitos regulamentares de "obstáculo em estágio final" a "contribuição de design em estágio inicial". O movimento em direcção a uma abordagem “orientada para o registo” significa que o próprio protótipo se tornará a base para o registo, sem modificações disruptivas posteriores, com o objectivo de um lançamento no mercado eficiente, fiável e rápido.
Por que confiar neste guia? Experiência prática dos especialistas em fabricação da LS
Existem vários milhares de artigos online sobre o tópico de prototipagem de dispositivos médicos - então por que você deveria gastar seu tempo lendo este? O que compartilhamos aqui não vem de uma definição de livro didático, mas sim de algumas diretrizes práticas vinculadas às rigorosas restrições da ISO 13485 e ISO9001 sistema e validado através de inúmeras cirurgias e resultados de testes.
Por mais de uma década, nossa equipe fabricou mais de 50.000 protótipos personalizados atendendo aos ISO 13485 para dispositivos médicos requisitos do sistema de qualidade. Cada projeto nos deu uma compreensão mais profunda de como definir os parâmetros de corte para ligas de magnésio biodegradáveis sem danos térmicos, como manter a estabilidade em estruturas de paredes finas durante o microfresamento e como implementar simultaneamente os requisitos de gerenciamento de risco e engenharia de usabilidade em cada etapa da iteração.
Confie em nós, o que você lê aqui é a metodologia central que usamos diariamente para superar desafios. Deixe-nos trabalhar juntos para transformar suas ideias inovadoras com eficiência e confiabilidade em produtos confiáveis.

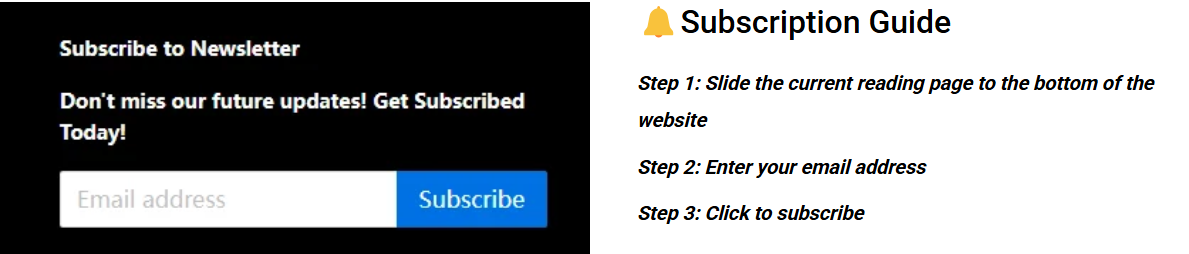
Figura 1: Protótipo abrangente para verificação de funcionalidade pela LS Manufacturing
Por que os protótipos de dispositivos médicos deveriam ir além da “validação funcional”?
O objetivo final do protótipo de dispositivo médico não é apenas ser um modelo “funcional”, mas um “ protótipo de produto ” que seja capaz de passar por todos os difíceis processos de registro e aprovação e ser aplicado com segurança no corpo humano. Portanto, o escopo de sua validação deve incluir o ciclo de vida completo dos riscos de uso.
- Tolerância à esterilidade: um protótipo pode ter função motora perfeita, mas não pode suportar processos repetidos de esterilização, como altas temperaturas e pressões, irradiação ou imersão química . O envelhecimento do material pode degradar o seu desempenho e causar infecção clínica. Os materiais compatíveis devem ser selecionados e validados durante a fase de protótipo .
- Visão geral da biocompatibilidade: As peças que entram em contato direto ou indireto com os pacientes devem ser feitas de materiais não tóxicos e não alérgicos . Esta substituição por materiais biocompatíveis posteriormente no processo de projeto pode afetar suas propriedades mecânicas e exigir um redesenho estrutural completo.
- Segurança e EMC (Compatibilidade Eletromagnética): No caso de dispositivos ativos, os protótipos devem considerar, antecipadamente, isolamento elétrico, corrente de fuga e outros indicadores de segurança para evitar, durante a operação, influenciar outros equipamentos sem ser influenciado por interferências externas. A retificação posterior é paga com um preço astronomicamente alto, e essa é uma necessidade a ser enfrentada no registro e nos testes.
Incorporando os requisitos de conformidade regulatória no desenvolvimento de protótipos de dispositivos médicos é, na verdade, uma abordagem proativa de gerenciamento de riscos. Isto evitaria alterações drásticas no design devido a problemas de funcionalidade que surgem durante o registo e os testes ou a validação clínica - poupando fundamentalmente muito tempo e dinheiro - e funciona como a pedra angular para acelerar o lançamento do produto .
Como a certificação ISO 13485 impacta o sistema de qualidade para desenvolvimento de protótipos?
Protótipo ISO 13485 eleva o processo de uma atividade potencialmente aleatória para um processo controlado, rastreável e vital que proporciona confiança precoce na segurança e eficácia do produto final. Requer um sistema de qualidade robusto desde a fase de conceito em diante. Isto se reflete particularmente em:
Controles rígidos de projeto e gerenciamento de documentação
Para a prototipagem, é necessário ter documentação de entrada, saída, revisão e alteração do projeto de acordo com a norma ISO 13485. São necessárias especificações totalmente documentadas, desde especificações de requisitos do cliente até registros de revisão de desenhos e conclusões de revisão de projeto. Isto também fornece consistência entre o protótipo e a intenção do projeto e forma um “histórico de projeto” útil, fornecendo evidências diretas para pedidos de registro subsequentes.
Fabricação Controlada e Rastreabilidade
Este padrão requer verificação e controle para os principais processos de prototipagem. Por exemplo, em termos dos materiais de qualidade médica envolvidos, devem ser fornecidos certificados de qualificação do fornecedor e registos de inspecção recebida ; também envolve configuração e confirmação dos parâmetros do equipamento de processamento, como espessura da camada e potência do laser em Impressão 3D . Isto garantiria consistência e repetibilidade neste processo de prototipagem e fornecer uma base clara para replicação ou iteração futura.
Integração antecipada da gestão de riscos
As atividades de gestão de riscos devem começar suficientemente cedo durante a prototipagem para identificar riscos potenciais associados ao design, materiais e processos para os quais medidas de controle devem ser implementadas. Nesse sentido, obriga a equipe a pensar antecipadamente nos requisitos ligados à segurança, como limpeza e esterilização e biocompatibilidade , integrar as soluções no projeto e fabricação do protótipo , reduzindo o potencial de grandes alterações de projeto posteriormente.
O valor proveniente de um sistema de qualidade ao longo de todo o processo de prototipagem vai muito além da obtenção de um certificado na ISO 13485 . Isto produzirá, para o próprio protótipo, uma estrutura padronizada e transparente ; não apenas uma “amostra” funcional, mas um “ pré-produto ” confiável, com dados completos e com risco controlado.
Seleção de materiais de qualidade médica que atendem aos requisitos de biocompatibilidade?
A seleção é o primeiro obstáculo na determinação da biocompatibilidade e segurança do produto no desenvolvimento do protótipo do dispositivo médico . A seleção de um material apropriado minimiza os riscos no registro, mas o mais importante é garantir a segurança do paciente. Para tornar clara a lógica de seleção, as principais considerações são comparadas abaixo.
| Dimensões de consideração | Caminho Básico: Seleção de Materiais Certificados |
Caminho Avançado: Avaliação Biológica de Materiais |
| Princípio | O uso de materiais de qualidade médica com certificação madura vem em primeiro lugar, como USP Classe VI ou ISO 10993. | Se for utilizado um material inovador, será necessária uma avaliação biológica completa de acordo com as normas ISO 10993 . |
|
Cenários Aplicáveis |
Aplica-se à maioria dos materiais maduros, de baixo risco e com uma rota clara e rápida. | Aplica-se a materiais novos e inovadores ou a cenários de interação humano-humano completamente novos, de maior risco e custo. |
| Evidências principais | Certificados de certificação e relatórios de teste totalmente preenchidos do fornecedor do material. |
Comissionar um laboratório devidamente equipado e qualificado para realizar o conjunto total ou parcial de testes de segurança exigidos. |
| Nosso suporte | Fornecemos correspondência rápida e recomendações com base em um banco de dados validado de materiais de qualidade médica , juntamente com consultoria sobre esquemas de avaliação e suporte para testes. | Apoiamos os clientes na mitigação dos riscos de compliance ao longo de todo o processo. |
Recomendamos fortemente o planejamento da biocompatibilidade desde os estágios iniciais da prototipagem, selecionando materiais pré-certificados de bancos de dados validados para minimizar a incerteza . Quando for necessário cobrir necessidades inovadoras, todo o percurso da avaliação biológica será planeado com muita antecedência. Isto evitaria atrasos no registo e perturbações nos projetos devido a questões materiais desde o início e estabeleceria as bases para a segurança e o rápido lançamento de produtos no mercado.

Figura 2: Controle volumétrico preciso para protótipos médicos da LS Manufacturing
Quais padrões os protótipos em diferentes estágios clínicos devem atender?
A maioria das pessoas interpreta mal prototipagem de dispositivos médicos como uma atividade em que uma versão de um protótipo tenta atender a todas as necessidades. Isso geralmente resulta no desperdício de recursos no uso ou na falta de padrões. O que a ciência apoia precisamente em cada passo - desde o conceito até à validação clínica - é a realização de protótipos "perfeitos", baseados nos objectivos das diferentes fases clínicas.
| Estágio Clínico | Protótipo de metas principais | Padrões e estratégias de produção |
| Prova de conceito | Verifique a viabilidade do conceito de design o mais rápido possível. | Métodos econômicos e rápidos, como a impressão 3D, podem atingir funções essenciais. Os materiais são ilimitados; agora é a hora de uma iteração rápida. |
| Teste Funcional |
Conduza testes de engenharia abrangentes de protótipos. |
Validação completa do desempenho e confiabilidade do produto usando protótipos que são representações aproximadas do tamanho, materiais e desempenho do produto. |
| Testes em animais | O primeiro passo do procedimento consiste em avaliar a segurança do produto em questão e a sua biocompatibilidade . | Deve ser preparado a partir de material biocompatível de qualidade médica após processamento asséptico para que os testes sejam válidos. |
| Validação Clínica | Os dados de segurança e eficácia devem ser obtidos em ensaios realizados em humanos. | O protótipo deve ser representativo do produto final e estar em conformidade com normas de dispositivos médicos no que diz respeito ao desempenho, materiais e processos de fabricação. |
De modo geral, a prototipagem de dispositivos médicos funciona de forma eficaz com uma abordagem dinâmica, mas progressiva. Desde a fase "económica" de prova de conceito até à fase de "quase-comercialização" , com validação clínica , cada estágio do projeto do protótipo deve definir determinados objetivos com padrões correspondentes. Tal estratégia manterá eficazmente os custos de I&D na fase inicial sob controlo, garantindo ao mesmo tempo que a integridade e a fiabilidade da cadeia de dados do protótipo são garantidas, evitando assim atrasos ou falhas no projecto devido a padrões de protótipos incompatíveis.
Como a precisão e a capacidade de fabricação podem ser equilibradas no protótipo de instrumentos cirúrgicos?
No processo de protótipo de instrumentos cirúrgicos desenvolvimento, o objetivo é não apenas alcançar melhor precisão funcional, mas também provar que seu design pode ser transformado de forma estável e econômica em produtos qualificados produzidos em massa. Os princípios de design para a capacidade de fabricação devem receber atenção prioritária. Portanto, os seguintes pontos devem ser levados em consideração:
Simplificação Estrutural e Otimização de Montagem
Ao garantir a funcionalidade, o número de peças deve ser minimizado e estruturas internas complexas evitadas. Por exemplo, a tecnologia de impressão 3D integrada poderia ser usada no lugar das estruturas tradicionais de montagem de várias peças ou designs de encaixe com travamento automático poderiam ser adotados em vez da fixação por parafuso. Ao fazê-lo, a dificuldade e o tempo de montagem posterior podem ser bastante reduzidos, melhorando assim a eficiência e a consistência da produção.
Combinando Processos de Fabricação e Design de Tolerância
Na etapa de prototipagem devem ser considerados os processos envolvidos na produção em massa, como moldagem por injeção de precisão e Usinagem de 5 eixos , e devem ser estabelecidas tolerâncias razoáveis. Não é necessário buscar precisão extrema se as dimensões do acoplamento não forem críticas ; caso contrário, o custo do processamento aumentará acentuadamente. Os projetistas precisam compreender os limites de capacidade dos diferentes processos e deixar margens razoáveis para erros de fabricação, ao mesmo tempo em que atendem aos requisitos clínicos.
Viabilidade de produção em massa de materiais e tratamentos de superfície
A seleção de materiais no caso de um protótipo deve atender não apenas aos requisitos de biocompatibilidade e propriedades mecânicas, mas também considerar a estabilidade da cadeia de abastecimento e o custo na produção em massa. Enquanto isso, tratamentos de superfície especiais, como revestimento antibacteriano, devem poder ser implementados de maneira estável e uniforme em lotes de peças, em vez de amostras de laboratório.
Um protótipo bem-sucedido de um instrumento cirúrgico incorpora considerações de capacidade de fabricação desde o início. Ele identifica e otimiza possíveis problemas de fabricação, qualidade e custos para produção em larga escala . A ideia é evitar a concepção de um produto “perfeito” que seja improdutível ou demasiado caro de fabricar, e também garantir que a transição do protótipo para a produção em massa seja suave.
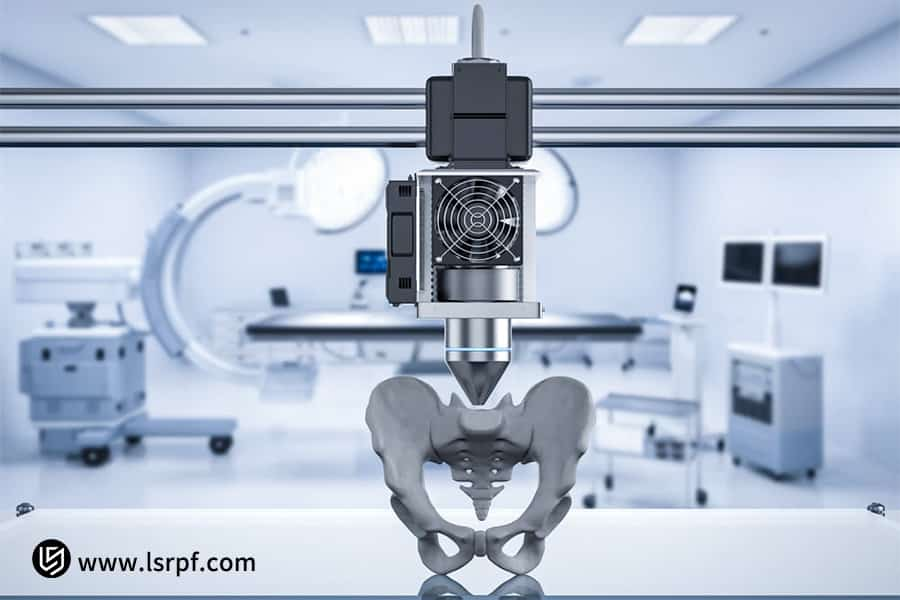
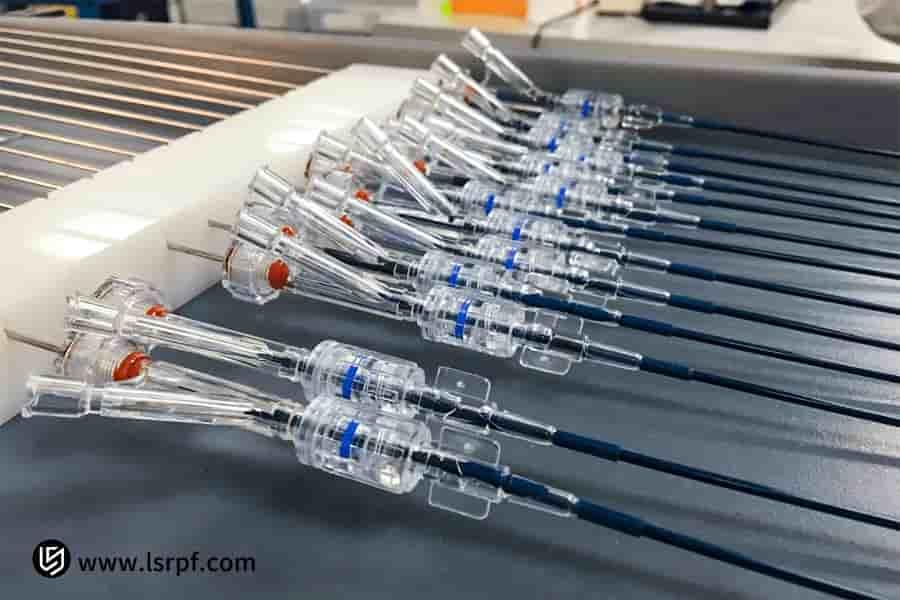
Figura 3: Desenvolvimento acelerado de implantes cirúrgicos sob medida pela LS Manufacturing
Como a tecnologia de prototipagem rápida facilita a inovação em dispositivos médicos?
O valor mais importante prototipagem rápida para dispositivos médicos é que ele pode encurtar o período desde o projeto conceitual até a verificação física, fornecendo uma plataforma muito eficaz para tentativa e erro e iteração. Entre estas tecnologias, a impressão 3D de qualidade médica está a desempenhar um papel revolucionário, com as suas vantagens e requisitos particularmente refletidos em:
- Alcançando Estruturas Complexas e Personalização Personalizada: Microcanais complexos e estruturas ósseas trabeculares porosas, difíceis de processar por métodos tradicionais, podem ser facilmente produzidos com impressão 3D de nível médico . Guias cirúrgicas e implantes personalizados, portanto, podem ser fabricados para se adaptarem exatamente à anatomia do paciente, um desenvolvimento que contribui diretamente para a medicina de precisão.
- Integração de diversos materiais e funções: Estes modernos tecnologias de prototipagem rápida permitem que os componentes sejam fabricados a partir de uma variedade de materiais que variam entre rígidos e flexíveis e biodegradáveis, tudo dentro de um único componente. Por exemplo, um componente integrado que combina uma estrutura rígida com um selo macio pode ser impresso em uma única etapa para uso em modelos anatômicos que simulam órgãos reais ou protótipos de dispositivos complexos de administração de medicamentos.
- Atendendo a requisitos específicos de aplicações médicas: A segurança e a conformidade nunca podem ser sacrificadas na prototipagem rápida de dispositivos médicos , não importa quanta velocidade esteja em jogo. Os materiais devem ser biocompatíveis e o próprio processo de impressão deve ser validado de forma a garantir consistência lote a lote e rastreabilidade ao longo de todo o processo de acordo com os requisitos do sistema de qualidade .
Estas são uma classe de tecnologias de prototipagem rápida em que impressão 3D de nível médico permite que a equipe de P&D explore projetos anteriormente impossíveis a um custo menor e em tempo recorde. O controle rigoroso sobre materiais e processos garante que a inovação siga o caminho da conformidade desde o estágio inicial até a validação clínica e registro do produto.
Como a LS Manufacturing ajuda os instrumentos cirúrgicos minimamente invasivos a superar o gargalo tecnológico?
O valor central da I&D de dispositivos médicos inovadores que oferecemos está relacionado com a sua serviços de prototipagem de dispositivos médicos em ajudar os clientes a superar os principais gargalos tecnológicos no lançamento de seus produtos. T A seguir está uma ilustração de caso típico que demonstra a aplicação do Protótipo médico da LS Manufacturing abordagem:
Desafio do cliente
No processo de desenvolvimento de um novo tipo de instrumento cirúrgico minimamente invasivo – um dispositivo de anastomose intracavitária – uma empresa inovadora encontrou enormes obstáculos durante testes em animais. O mecanismo de transmissão central demonstrou um atraso significativo na operação e não pôde fornecer aos cirurgiões um controle eficaz e preciso da ação da anastomose. Restringido pelo processo de fabricação tradicional, não havia mais espaço para otimização adicional devido à sua complicada estrutura interna de transmissão.
Solução de Fabricação LS
Intervindo, nossa equipe de engenharia abandonou imediatamente o método de usinagem tradicional. Nós empregamos aço inoxidável de qualidade médica Tecnologia de impressão 3D , fabricando um sistema de transmissão de uma etapa e uma peça com um caminho mecânico superior e folga mínima extrema. Isto não resolveu apenas o problema do atraso; melhorias adicionais tiveram o eletropolimento aplicado nesta complexa cavidade moldada de peça única , proporcionando-lhe um acabamento superficial muito superior aos padrões e atendendo perfeitamente aos requisitos extremamente elevados de esterilidade e limpeza para instrumentos cirúrgicos.
Resultados e Valor
Em testes subsequentes em animais, o protótipo recém-fabricado funcionou perfeitamente e a velocidade de resposta operacional e a precisão do instrumento melhoraram cerca de 60% , ganhando elogios de especialistas clínicos. Este avanço tecnológico avançou diretamente o cronograma geral do projeto do cliente em pelo menos 5 meses e economizou mais de 2 milhões de RMB em custos de P&D incorridos em repetidas tentativas e erros e modificações de moldes.
Aplicamos tecnologias avançadas, como impressão 3D de nível médico, para superar limitações comuns de estrutura, material e desempenho de instrumentos cirúrgicos minimamente invasivos para nossos clientes. O que pareciam desafios técnicos impossíveis tornou-se a chave para a competitividade do produto, garantindo valiosas janelas de tempo de colocação no mercado e enormes vantagens de custos para os nossos clientes.

Figura 4: Dosagem de precisão na fabricação de protótipos médicos pela LS Manufacturing
Que tipo de documentação técnica o desenvolvimento de protótipos em dispositivos médicos exige?
Completo documentação técnica é a base do registro bem-sucedido de dispositivos médicos. Serve principalmente para documentar de forma abrangente o processo de controle do projeto e fornecer evidências sobre a segurança e eficácia do produto. Isto não será apenas um roteiro para o desenvolvimento interno, mas também servirá como prova para as agências reguladoras da capacidade de desenvolvimento sistemático e compatível da empresa. Incluirá, entre outros, os seguintes documentos principais:
- Projetar documentos de entrada e saída: Este é o início do sistema de documentação: projetar entradas, que devem registrar as necessidades do usuário, funções clínicas, indicadores de desempenho e padrões regulatórios de maneira clara. Os resultados do projeto incluirão desenhos de produtos, especificações técnicas, listas de peças, etc. Cada entrada deve ser verificada para ter uma saída correspondente.
- Certificação de materiais e documentação de biocompatibilidade: Certificações de fornecedores e certificados de materiais de todos os materiais de grau médico, juntamente com avaliação de biocompatibilidade ou relatórios de testes, conforme relevante para partes da USP Classe VI ou ISO 10993, devem estar disponíveis. Isto está diretamente relacionado ao estabelecimento da biocompatibilidade do produto.
- Registros de Validação do Processo de Fabricação: Demonstram que o processo de fabricação do protótipo é consistente e controlável para cada processo crítico envolvido em sua criação, como Parâmetros de impressão 3D ou processos de esterilização , por meio de registros detalhados de parâmetros de processo, certificados de calibração de equipamentos e relatórios de inspeção de primeiro artigo.
Em outras palavras, significa a criação de documentação técnica como atividade básica que corre paralelamente à prototipagem e prepara para o andamento eficiente do projeto; não é uma reflexão tardia. Um bom controle de projeto O sistema de documentação, como a “certidão de nascimento” do produto, mostra claramente a trajetória do projeto desde o conceito até o protótipo.
Como planejar o caminho do pedido de registro durante a fase de prototipagem?
Com base no bom trabalho de preparação do pedido de registro , acelerar o desenvolvimento de dispositivos médicos pode ter certeza e, nesse processo, cada dado gerado se tornará um forte suporte para futuros documentos de registro. Ou seja, os três níveis seguintes devem ser planeados sistematicamente:
Definindo claramente os requisitos relativos à evidência de registro
A fase de entrada do projeto do protótipo exige uma análise aprofundada dos requisitos regulatórios do mercado-alvo. Os principais itens que devem ser verificados durante a revisão dos registros, como indicadores de desempenho, biocompatibilidade e segurança elétrica, são traduzidos em parâmetros técnicos específicos a serem verificados pelo protótipo. Isso garantiria o desenvolvimento de um protótipo no caminho certo e compatível desde o início.
Transforme os dados de validação do protótipo em evidências de registro
O protótipo deverá passar por testes funcionais, de vida útil e de usabilidade que atendam aos requisitos do sistema de qualidade . Todos os testes devem ser feitos com um protocolo padrão pré-aprovado, que deve incluir um registro completo dos dados brutos e um relatório padronizado. Serão dados altamente controlados que poderão então ser submetidos diretamente como evidência central para validação futura do projeto, evitando assim a repetição de testes.
Estabeleça um sistema transparente para documentação do histórico do projeto
Deve fornecer um registro completo do processo que flui desde a entrada do projeto até a revisão, alterações e saída. Este sistema de documentação formado naturalmente no processo de controle de projeto pode ser a melhor evidência para provar às agências reguladoras que o processo de projeto é rigoroso e controlado, o que pode melhorar significativamente a eficiência e a taxa de sucesso das revisões de registro.
Em outras palavras, planejar pedido de registro a integração na fase de protótipo é a melhor alavanca para acelerar o desenvolvimento de dispositivos médicos , na medida em que reduz fortemente os elevados custos e os atrasos incorridos nas fases posteriores do projecto devido a dados de registo suplementares, ao mesmo tempo que melhora a normalização e a taxa de sucesso de todo o processo de I&D desde o início, estabelecendo uma base sólida para o lançamento rápido e estável de produtos no mercado
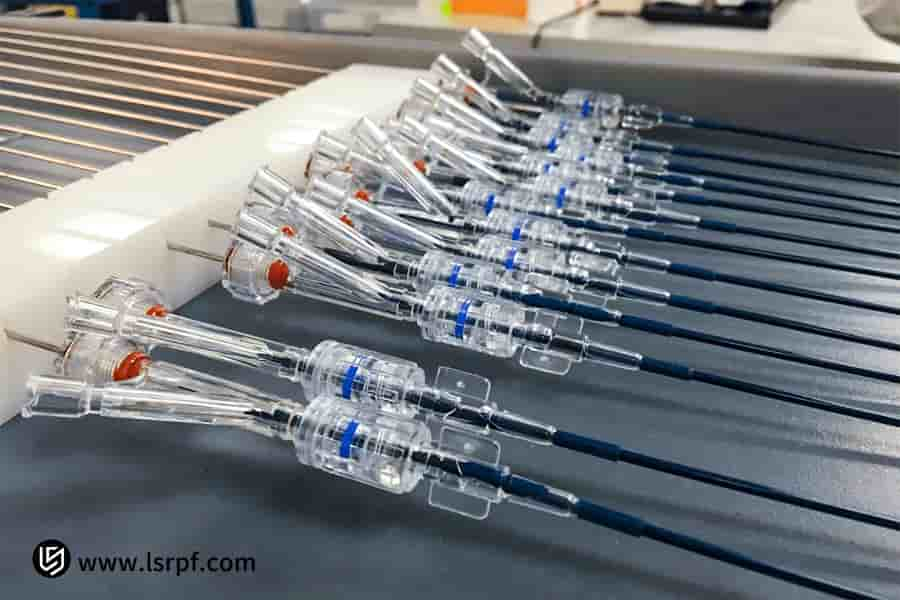
Figura 5: Protótipo de 360 graus para validação funcional pela LS Manufacturing
Perguntas frequentes
1. Que requisitos específicos devem ser seguidos durante o desenvolvimento de protótipos de dispositivos médicos?
Além disso, para além da funcionalidade básica, é necessário abordar proativamente o cumprimento das normas específicas para dispositivos médicos. Aplicamos rigorosamente os sistema de qualidade da ISO 13485 para garantir que esses protótipos atendam aos requisitos regulatórios de biocompatibilidade, tolerância à esterilização, segurança elétrica e outros aspectos logo no início de seu registro.
2. Quanto tempo leva desde o conceito até a obtenção do primeiro protótipo funcional?
Depende da complexidade do dispositivo. Dispositivos relativamente simples levam cerca de 2 a 3 semanas, enquanto dispositivos mais complexos, com transmissões de precisão e componentes eletrônicos, levam de 4 a 6 semanas . Temos um canal rápido para atender com flexibilidade às necessidades urgentes de P&D e garantir totalmente o cronograma do seu projeto.
3. É possível fabricar pequenos lotes de dispositivos para ensaios clínicos?
Obviamente, um de nossos vários serviços é a fabricação de pequenos lotes de dispositivos para ensaios clínicos , variando de 10 a 100 unidades . A fabricação foi por padrões de fabricação de dispositivos médicos , e cada unidade será fabricada com os exigentes desempenho, qualidade e consistência para ensaios clínicos.
4. Como garantir a biocompatibilidade dos materiais dos protótipos?
Controlamos os riscos desde a fonte através da seleção rigorosa de materiais de qualidade médica com certificações oficiais , como ISO 10993 ou USP Classe VI. Documentos completos de certificação de material podem ser fornecidos junto com o protótipo, fornecendo evidências substanciais para sua avaliação de biocompatibilidade.
5. Como você protege nosso IP durante o processo de prototipagem?
A segurança da informação é a nossa tábua de salvação. Cada projeto começa com um acordo de confidencialidade juridicamente vinculativo e, internamente, aplicamos um rigoroso sistema de gestão de hierarquia de dados e controle de acesso. Caso solicitado pelo cliente, também poderão ser estabelecidos firewalls físicos e de informação.
6. Que tipo de protótipo de dispositivo médico você apoia?
Os serviços oferecidos pela nossa empresa vão desde dispositivos ativos, como equipamentos de diagnóstico, até passivos, incluindo instrumentos cirúrgicos, implantes e dispositivos não implantáveis . LS Fabricação é bem versado no que diz respeito aos regulamentos e processos associados a vários produtos.
7. Como disponibilizar os dados do protótipo para utilização em pedidos de posterior registro?
Além dos protótipos, fornecemos um pacote completo de evidências de qualidade, que inclui registros detalhados de produção, relatórios de inspeção de processos e dados de testes de desempenho . Todos são gerados de acordo com especificações e podem ser diretamente utilizados como material de verificação de projeto para apoiar pedidos de registro.
8. Como iniciar um projeto de protótipo de dispositivo médico?
O processo para começar é bastante simples: basta preencher alguns esboços de conceito inicial ou requisitos técnicos, e garantiremos que um engenheiro sênior entre em contato com você dentro de um dia útil para discutir as soluções técnicas em profundidade e fornecer-lhe uma avaliação e cotação inicial do projeto.
Resumo
Os protótipos de dispositivos médicos são muito mais do que uma realização técnica; eles são a base do gerenciamento de riscos, da conformidade regulatória e do sucesso comercial. Encontrar o parceiro de prototipagem certo estabelece uma base sólida para todo o ciclo de vida do produto.
Portanto, se você deseja acelerar a P&D e ao mesmo tempo reduzir os riscos de registro, por favor entre em contato com nossos especialistas em dispositivos médicos hoje para uma "solução de prototipagem orientada para registro" para o seu projeto! Deixe-nos aplicar nossa experiência profissional na fabricação de dispositivos médicos para proteger sua jornada de inovação.
📞Telefone: +86 185 6675 9667
📧E-mail: info@longshengmfg.com
🌐Site: https://lsrpf.com/
Isenção de responsabilidade
O conteúdo desta página é apenas para fins informativos. A LS Manufacturing não faz representações ou garantias, expressas ou implícitas, relativamente à exatidão, integridade ou validade das informações. Não se deve inferir que fornecedores ou fabricantes terceiros fornecerão parâmetros de desempenho, tolerâncias geométricas, características específicas de design, qualidade e tipo de material, ou processos através da rede LS Manufacturing. O comprador é o único responsável por esta informação. Para cotações de peças, especifique os requisitos exatos para essas peças. Entre em contato conosco para mais informações .
Equipe de Fabricação LS
LS Manufacturing é uma empresa líder do setor especializada em soluções de fabricação customizadas. Com mais de 20 anos de experiência atendendo mais de 5.000 clientes, nos concentramos em alta precisão Usinagem CNC , fabricação de chapas metálicas , Impressão 3D , moldagem por injeção , estampagem de metal e outros serviços de fabricação completos.
Nossa fábrica possui mais de 100 centros de usinagem de cinco eixos de última geração e possui certificação ISO 9001:2015. Fornecemos soluções de fabricação rápidas, eficientes e de alta qualidade para clientes em mais de 150 países e regiões em todo o mundo. Quer se trate de produção em pequenos lotes ou personalização em massa, podemos atender às suas necessidades em 24 horas. Escolher a LS Manufacturing significa escolher eficiência, qualidade e profissionalismo.
Para mais informações, visite nosso site: www.lsrpf.com .