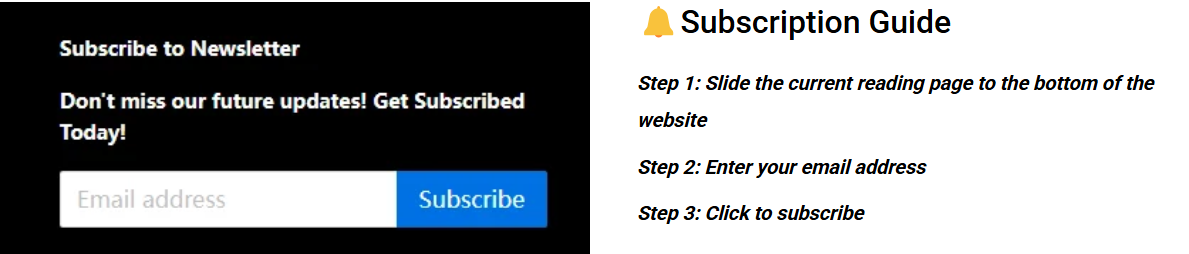
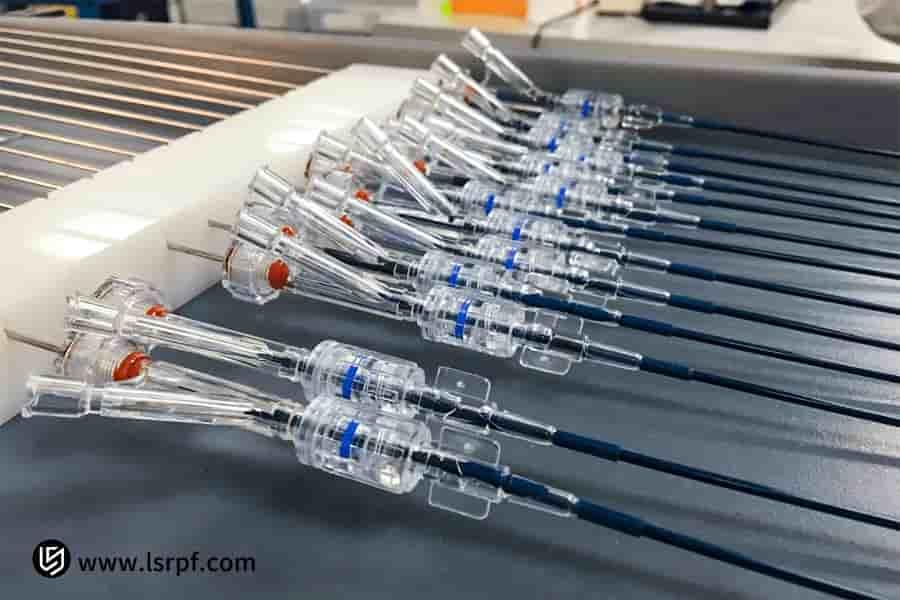
Prototype de dispositif médical La mission principale de garantir la conformité réglementaire est fondamentalement différente des prototypes d'ingénierie générale. En fait, c’est la cause première des idées fausses sur la lenteur des itérations. Dans le modèle traditionnel, on sépare la vérification fonctionnelle et réglementaire ; ainsi, face à des défis réglementaires tels que la biocompatibilité et la sécurité électrique, des modifications drastiques doivent être apportées ultérieurement au prototype, retardant considérablement les essais cliniques et l'enregistrement.
La stratégie « Registration-Oriented Prototyping » de LS Manufacturing intègre les exigences réglementaires de manière systématique dès la phase de conception. Il place les normes en tête de sa liste de priorités pour garantir le respect des éléments clés d'enregistrement en conjonction avec la réalisation fonctionnelle du prototype, de sorte que le prototype soit qualifié pour les tests de validation clinique et d'enregistrement, garantissant ainsi le premier succès du lancement du produit. Pour vous faire gagner du temps, voici un bref aperçu des principales conclusions.
Référence rapide sur le prototypage de dispositifs médicaux
| Module | Clé à retenir |
| Concept de base | Créez des « prototypes dirigés par l'enregistrement » qui intègrent des fonctions conformes à la réglementation. |
| Points douloureux traditionnels | L’introduction d’exigences réglementaires tard dans le processus entraîne des modifications répétées du prototype, retardant ainsi la mise sur le marché. |
| Éléments clés | La biocompatibilité, l’ingénierie d’utilisabilité et la gestion des risques doivent être abordées ensemble lors de la phase de prototypage. |
| Solution | Obtenez la bonne conception du premier coup grâce à une surveillance réglementaire proactive et en travaillant en parallèle. |
| Valeur ultime | Réduire considérablement le risque d’enregistrement et raccourcir considérablement le cycle total de lancement du produit. |
Le tableau suivant illustre comment accélérer le développement de dispositifs médicaux en déplaçant les exigences réglementaires de « l'obstacle à un stade avancé » à « une contribution à la conception à un stade précoce ». L'évolution vers une approche « orientée vers l'enregistrement » signifie que le prototype lui-même deviendra la base de l'enregistrement, sans modifications perturbatrices ultérieures, dans le but d'un lancement sur le marché efficace, fiable et rapide.
Pourquoi faire confiance à ce guide ? Expérience pratique des experts de fabrication LS
Il existe plusieurs milliers d'articles en ligne sur le sujet du prototypage de dispositifs médicaux. Alors pourquoi devriez-vous passer votre temps à lire celui-ci ? Ce que nous partageons ici ne provient pas d'une définition de manuel mais plutôt de quelques lignes directrices pratiques liées par les contraintes rigoureuses de la norme ISO 13485 et ISO9001 système et validé par d’innombrables interventions chirurgicales et résultats de tests.
Depuis plus d'une décennie, notre équipe a fabriqué plus de 50 000 prototypes personnalisés répondant aux ISO 13485 pour les dispositifs médicaux exigences du système qualité. Chaque projet nous a permis de mieux comprendre comment définir les paramètres de coupe pour les alliages de magnésium biodégradables sans dommages thermiques, comment maintenir la stabilité des structures à parois minces pendant le microfraisage et comment mettre en œuvre simultanément les exigences de gestion des risques et d'ingénierie d'utilisabilité à chaque étape de l'itération.
Faites-nous confiance, ce que vous lisez ici est la méthodologie de base que nous utilisons quotidiennement pour surmonter les défis. Travaillons ensemble pour transformer vos idées novatrices avec efficacité et fiabilité en produits dignes de confiance.

Figure 1 : Prototype complet pour la vérification des fonctionnalités par LS Manufacturing
Pourquoi les prototypes de dispositifs médicaux devraient-ils aller au-delà de la « validation fonctionnelle » ?
L'objectif ultime du prototype de dispositif médical n'est pas seulement d'être un modèle « fonctionnel », mais un « prototype de produit » capable de passer avec succès tous les processus difficiles d'enregistrement et d'approbation et d'être appliqué en toute sécurité sur le corps humain. Le périmètre de sa validation doit donc inclure le cycle de vie complet des risques d’utilisation.
- Tolérance de stérilité : un prototype peut avoir une fonction motrice parfaite mais ne peut pas supporter des processus de stérilisation répétés, tels que des températures et des pressions élevées, une irradiation ou une immersion chimique . Le vieillissement du matériau peut dégrader ses performances et provoquer une infection clinique. Les matériaux conformes doivent être sélectionnés et validés lors de la phase de prototype .
- Aperçu de la biocompatibilité : Les pièces entrant en contact direct ou indirect avec les patients doivent être constituées de matériaux non toxiques et non allergiques . Ce remplacement par des matériaux biocompatibles plus tard dans le processus de conception peut affecter leurs propriétés mécaniques et nécessiter une refonte structurelle complète.
- Sécurité et CEM (Compatibilité Electromagnétique) : Dans le cas de dispositifs actifs, les prototypes doivent prendre en compte, au préalable, l'isolation électrique, le courant de fuite et d'autres indicateurs de sécurité pour éviter, pendant le fonctionnement, d'influencer d'autres équipements sans être influencés par des interférences externes. La rectification ultérieure est payée à un prix astronomiquement élevé, et c'est une nécessité à laquelle il faut faire face lors de l'enregistrement et des tests.
Intégrer les exigences de conformité réglementaire Le développement de prototypes de dispositifs médicaux constitue en réalité une approche proactive de gestion des risques. Cela permettrait d'éviter des changements de conception drastiques dus à des problèmes de fonctionnalité survenant lors de l'enregistrement et des tests ou de la validation clinique - ce qui permettrait d'économiser beaucoup de temps et d'argent - et constituerait la pierre angulaire de l'accélération du lancement du produit .
Quel est l'impact de la certification ISO 13485 sur le système qualité pour le développement de prototypes ?
Prototype ISO 13485 élève le processus d'une activité potentiellement aléatoire à un processus contrôlé, traçable et vital qui fournit une confiance précoce dans la sécurité et l'efficacité du produit final. Cela nécessite un système qualité robuste dès la phase de conception. Cela se reflète notamment dans :
Contrôles de conception stricts et gestion de la documentation
Pour le prototypage, il est nécessaire de disposer d'une documentation sur les entrées, sorties, révisions et modifications de la conception conformément à la norme ISO 13485. Des spécifications entièrement documentées sont requises, depuis les spécifications des exigences du client jusqu'aux enregistrements de révision des dessins et aux conclusions de l'examen de la conception. Cela assure également une cohérence entre le prototype et l'intention de conception et forme un « historique de conception » utile, fournissant une preuve directe pour les demandes d'enregistrement ultérieures.
Fabrication contrôlée et traçabilité
Cette norme exige la vérification et le contrôle des processus clés de prototypage. Par exemple, en ce qui concerne les matériaux de qualité médicale concernés, les certificats de qualification des fournisseurs et les dossiers d'inspection à la réception doivent être fournis ; cela implique également la configuration et la confirmation des paramètres de l'équipement de traitement, tels que l'épaisseur de la couche et la puissance du laser. impression 3D . Cela garantirait cohérence et répétabilité dans ce processus de prototypage et donnent une base claire pour une réplication ou une itération future.
Intégration précoce de la gestion des risques
Les activités de gestion des risques doivent commencer suffisamment tôt pendant le prototypage pour identifier les risques potentiels associés à la conception, aux matériaux et aux processus pour lesquels des mesures de contrôle doivent être mises en œuvre. À cet égard, cela oblige l'équipe à réfléchir à l'avance aux exigences liées à la sécurité, telles que le nettoyage, la stérilisation et la biocompatibilité , à intégrer les solutions dans la conception et la fabrication du prototype , réduisant ainsi le risque de modifications majeures de la conception ultérieurement.
La valeur provenant d'un système de qualité tout au long du processus de prototypage va bien au-delà de la simple obtention d'un certificat ISO 13485 . Cela produira, pour le prototype lui-même, un cadre standardisé et transparent ; non seulement un « échantillon » fonctionnel, mais aussi un « pré-produit » fiable, complet en données et dont les risques sont contrôlés.
Sélection de matériaux de qualité médicale répondant aux exigences de biocompatibilité ?
La sélection est le premier obstacle à la détermination de la biocompatibilité et de la sécurité du produit lors du développement du prototype de dispositif médical . La sélection d'un matériau approprié minimise les risques liés à l'enregistrement mais garantit surtout la sécurité des patients. Pour clarifier les logiques de sélection, les principales considérations sont comparées ci-dessous.
| Dimensions de considération | Parcours de base : sélection de matériaux certifiés |
Parcours avancé : évaluation biologique des matériaux |
| Principe | L'utilisation de matériaux de qualité médicale avec une certification mature passe en premier, comme USP Classe VI ou ISO 10993. | Si un matériau innovant est utilisé, une évaluation biologique complète selon les normes ISO 10993 sera requise. |
|
Scénarios applicables |
S'applique aux matériaux les plus matures, à faible risque et ayant un itinéraire clair et rapide. | S’applique aux matériaux nouveaux et innovants ou à des scénarios d’interaction homme-humain complètement nouveaux présentant des risques et des coûts plus élevés. |
| Preuve clé | Certificats de certification et rapports de test entièrement remplis du fournisseur de matériaux. |
Mise en service d'un laboratoire correctement équipé et qualifié pour effectuer l'ensemble complet ou partiel des tests de sécurité requis. |
| Notre soutien | Nous fournissons une correspondance rapide et des recommandations basées sur une base de données validée de matériaux de qualité médicale , ainsi que des conseils sur les programmes d'évaluation et l'assistance aux tests. | Nous aidons nos clients à atténuer les risques de non-conformité tout au long du processus. |
Nous recommandons fortement de planifier la biocompatibilité dès les premières étapes du prototypage, en sélectionnant des matériaux précertifiés dans des bases de données validées afin de minimiser l'incertitude . Là où des besoins innovants doivent être couverts, le parcours complet de l’évaluation biologique sera planifié longtemps à l’avance. Cela éviterait dès le début les retards dans l'enregistrement et les perturbations dans les conceptions dues à des problèmes matériels et jetterait les bases d'une sécurité et d'un lancement rapide des produits sur le marché.

Figure 2 : Contrôle volumétrique précis des prototypes médicaux par LS Manufacturing
À quelles normes les prototypes doivent-ils répondre à différents stades cliniques ?
La plupart des gens interprètent mal prototypage de dispositifs médicaux comme une activité dans laquelle une version d'un prototype tente de répondre à tous les besoins. Cela entraîne souvent un gaspillage de ressources lors de leur utilisation ou un manque de normes. Ce que la science soutient précisément à chaque étape, du concept à la validation clinique , c'est la création de prototypes « parfaits », basés sur les objectifs des différentes étapes cliniques.
| Stade clinique | Objectifs fondamentaux du prototype | Normes et stratégies de production |
| Preuve de concept | Vérifiez la faisabilité du concept de conception dès que possible. | Des méthodes économiques et rapides, comme l’impression 3D, peuvent réaliser des fonctions essentielles. Les matériaux sont illimités ; le moment est venu de procéder à une itération rapide. |
| Tests fonctionnels |
Effectuer des tests techniques complets sur les prototypes. |
Validation approfondie des performances et de la fiabilité du produit à l'aide de prototypes qui sont des représentations proches de la taille, des matériaux et des performances du produit. |
| Tests sur les animaux | La première étape de la procédure consiste à évaluer la sécurité du produit concerné et sa biocompatibilité . | Il doit être préparé à partir d’ un matériau biocompatible de qualité médicale après un traitement aseptique pour que les tests soient valides. |
| Validation clinique | Les données de sécurité et d'efficacité doivent être obtenues dans des essais menés chez l'homme. | Le prototype doit être représentatif du produit final et doit être conforme aux normes relatives aux dispositifs médicaux en ce qui concerne les performances, les matériaux et les processus de fabrication. |
De manière générale, le prototypage de dispositifs médicaux fonctionne efficacement avec une approche dynamique mais progressive. De l' étape de preuve de concept « économique » jusqu'à l'étape de « quasi-commercialisation » , avec validation clinique , chaque étape de la conception du prototype doit définir certains objectifs avec des normes correspondantes. Une telle stratégie permettra de contrôler efficacement les coûts de R&D à un stade précoce tout en garantissant l' intégrité et la fiabilité de la chaîne de données des prototypes , évitant ainsi les retards ou les échecs du projet en raison de normes de prototypes inadaptées.
Comment équilibrer précision et fabricabilité dans le prototype d’instruments chirurgicaux ?
En cours de prototype d'instruments chirurgicaux développement, l'objectif est non seulement d'obtenir une meilleure précision fonctionnelle, mais également de prouver que sa conception peut être transformée de manière stable et économique en produits qualifiés produits en série. Les principes de conception pour la fabricabilité doivent faire l'objet d'une attention prioritaire. Par conséquent, les points suivants doivent être pris en considération :
Simplification structurelle et optimisation de l'assemblage
Tout en garantissant la fonctionnalité, le nombre de pièces doit être minimisé et les structures internes complexes évitées. Par exemple, la technologie d'impression 3D intégrée pourrait être utilisée à la place des structures d'assemblage traditionnelles en plusieurs parties, ou des conceptions à encliquetage autobloquantes pourraient être adoptées au lieu de la fixation par vis. Ce faisant, les difficultés et le temps d'assemblage ultérieur peuvent être considérablement réduits, améliorant ainsi l'efficacité et la cohérence de la production.
Processus de fabrication adaptés et conception de tolérances
Au stade du prototypage, les processus impliqués dans la production de masse doivent être pris en compte, tels que le moulage par injection de précision et Usinage 5 axes , et des tolérances raisonnables doivent être fixées. Il n'est pas nécessaire de rechercher une précision extrême si les dimensions d'accouplement ne sont pas critiques ; sinon, le coût du traitement augmentera fortement. Les concepteurs doivent comprendre les limites de capacité des différents processus et laisser des marges raisonnables pour les erreurs de fabrication tout en répondant aux exigences cliniques.
Faisabilité de la production en série de matériaux et de traitements de surface
La sélection des matériaux dans le cas d'un prototype doit non seulement répondre aux exigences de biocompatibilité et de propriétés mécaniques, mais également tenir compte de la stabilité de la chaîne d'approvisionnement et du coût de la production de masse. Dans le même temps, des traitements de surface spéciaux, tels qu'un revêtement antibactérien, devraient pouvoir être appliqués de manière stable et uniforme sur des lots de pièces plutôt que sur des échantillons de laboratoire.
Un prototype réussi d’instrument chirurgical intègre dès le début des considérations de fabricabilité . Il identifie et optimise les problèmes possibles de fabrication, de qualité et de coût pour la production à grande échelle . L’idée est d’éviter de concevoir un produit « parfait » qui serait soit impossible à produire, soit trop coûteux à fabriquer, et également de garantir que la transition du prototype à la production de masse se fasse en douceur.
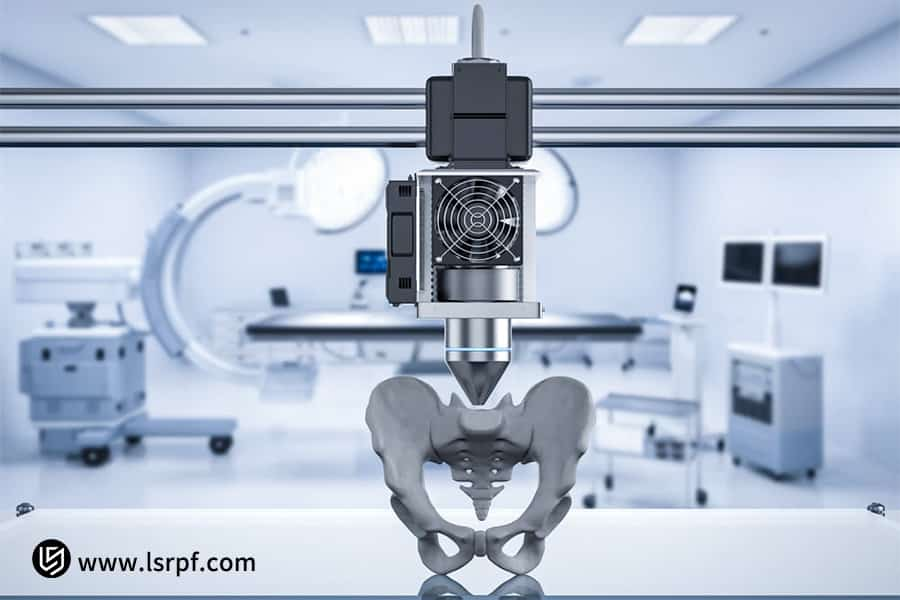
Figure 3 : Développement accéléré d’implants chirurgicaux sur mesure par LS Manufacturing
Comment la technologie de prototypage rapide facilite-t-elle l’innovation dans le domaine des dispositifs médicaux ?
La valeur la plus importante de prototypage rapide pour dispositifs médicaux est qu'il peut raccourcir la période de temps entre la conception conceptuelle et la vérification physique, fournissant ainsi une plate-forme très efficace pour les essais, les erreurs et les itérations. Parmi ces technologies, l’impression 3D de qualité médicale joue un rôle révolutionnaire, avec ses avantages et ses exigences qui se traduisent notamment par :
- Réalisation de structures complexes et personnalisation personnalisée : des microcanaux complexes et des structures osseuses trabéculaires poreuses, difficiles à traiter par les méthodes traditionnelles, peuvent facilement être produits avec l'impression 3D de qualité médicale . Des guides chirurgicaux et des implants personnalisés peuvent donc être fabriqués pour s'adapter exactement à l'anatomie du patient, un développement qui contribue directement à la médecine de précision.
- Intégration de plusieurs matériaux et fonctions : Ces modernes technologies de prototypage rapide permettent de fabriquer des composants à partir d'une gamme de matériaux allant du rigide au flexible en passant par le biodégradable, le tout dans un seul composant. Par exemple, un composant intégré combinant un cadre rigide avec un joint souple peut être imprimé en une seule étape pour être utilisé dans des modèles anatomiques simulant des organes réels ou des prototypes de dispositifs complexes d'administration de médicaments.
- Répondre aux exigences particulières des applications médicales : la sécurité et la conformité ne peuvent jamais être sacrifiées dans le prototypage rapide de dispositifs médicaux , quelle que soit la vitesse en jeu. Les matériaux doivent être biocompatibles et le processus d'impression lui-même doit être validé de manière à garantir la cohérence d'un lot à l'autre et la traçabilité tout au long du processus conformément aux exigences du système qualité .
Il s'agit d'une classe de technologies de prototypage rapide dans lesquelles impression 3D de qualité médicale permet à l’équipe R&D d’explorer des conceptions auparavant impossibles à moindre coût et en un temps record. Le contrôle rigoureux des matériaux et des processus garantit que l'innovation suit la voie de la conformité depuis la phase initiale jusqu'à la validation clinique et l'enregistrement du produit.
Comment LS Manufacturing aide-t-il les instruments chirurgicaux mini-invasifs à surmonter le goulot d'étranglement technologique ?
La valeur fondamentale de la R&D de dispositifs médicaux innovants que nous proposons concerne son services de prototypage de dispositifs médicaux en aidant les clients à surmonter les principaux goulots d'étranglement technologiques lors du lancement de leurs produits. T Ce qui suit est une illustration de cas typique qui démontre l'application de la Prototype médical LS Manufacturing approche:
Défi client
En développant un nouveau type d' instrument chirurgical mini-invasif - un dispositif d'anastomose intracavitaire - une entreprise innovante s'est heurtée à d'énormes obstacles lors des tests sur les animaux. Le mécanisme de transmission central a démontré un retard de fonctionnement important et n'a pas pu fournir aux chirurgiens un contrôle efficace et précis de l'action de l'anastomose. Limité par le processus de fabrication traditionnel, il n'y avait plus de place pour une optimisation supplémentaire en raison de sa structure de transmission interne complexe.
Solution de fabrication LS
En intervenant, notre équipe d’ingénierie a immédiatement abandonné la méthode d’usinage traditionnelle. Nous avons employé acier inoxydable de qualité médicale Technologie d'impression 3D , fabrication d'un système de transmission en une seule étape et d'une seule pièce avec un chemin mécanique supérieur et un jeu extrêmement minimal. Cela n’a pas seulement résolu le problème du décalage ; Une amélioration supplémentaire a été apportée à cette cavité moulée complexe d'une seule pièce par électropolissage , lui conférant un état de surface dépassant largement les normes et répondant parfaitement aux exigences extrêmement élevées de stérilité et de propreté des outils chirurgicaux.
Résultats et valeur
Lors d'essais ultérieurs sur des animaux, le prototype nouvellement fabriqué a parfaitement fonctionné et la vitesse de réponse opérationnelle et la précision de l'instrument se sont améliorées d'environ 60 % , gagnant les éloges des experts cliniques. Cette percée technologique a ainsi directement fait avancer le calendrier global du projet du client d'au moins 5 mois et a permis d'économiser plus de 2 millions de RMB en coûts de R&D liés aux essais et erreurs répétés et à la modification du moule.
Nous avons appliqué des technologies avancées, telles que l'impression 3D de qualité médicale, pour surmonter les limitations courantes de structure, de matériaux et de performances des instruments chirurgicaux mini-invasifs pour nos clients. Ce qui semblait être des défis techniques impossibles est devenu la clé de la compétitivité des produits, garantissant des délais de mise sur le marché précieux et d'énormes avantages en termes de coûts pour nos clients.

Figure 4 : Dosage de précision dans la fabrication de prototypes médicaux par LS Manufacturing
Quel type de documentation technique le développement de prototypes de dispositifs médicaux nécessite-t-il ?
Complet documentation technique est la pierre angulaire d’un enregistrement réussi des dispositifs médicaux. Il sert principalement à documenter de manière exhaustive le processus de contrôle de la conception et à fournir des preuves de la sécurité et de l'efficacité du produit. Ce ne sera pas seulement une feuille de route pour le développement interne, mais servira également de preuve aux agences de réglementation de la capacité de développement systématique et conforme de l'entreprise. Il comprendra, sans toutefois s'y limiter, les documents clés suivants :
- Documents d'entrée et de sortie de conception : c'est le début du système de documentation : les entrées de conception, qui doivent enregistrer de manière claire les besoins des utilisateurs, les fonctions cliniques, les indicateurs de performance et les normes réglementaires. Les résultats de la conception comprendront des dessins de produits, des spécifications techniques, des listes de pièces, etc. Chaque entrée doit être vérifiée pour avoir une sortie correspondante.
- Certification des matériaux et documentation sur la biocompatibilité : les certifications des fournisseurs et les certificats de matériaux de tous les matériaux de qualité médicale, accompagnés d'évaluations de biocompatibilité ou de rapports de tests pertinents pour les parties de l'USP Classe VI ou de l'ISO 10993, doivent être disponibles. Cela concerne directement l’établissement de la biocompatibilité du produit.
- Dossiers de validation du processus de fabrication : démontrer que le processus de fabrication du prototype est cohérent et contrôlable pour chaque processus critique impliqué dans sa création, tel que Paramètres d'impression 3D ou des processus de stérilisation , via des enregistrements détaillés des paramètres de processus, des certificats d'étalonnage des équipements et des rapports d'inspection du premier article.
En d’autres termes, cela signifie que la création de documentation technique est une activité de base parallèle au prototypage qui prépare à un avancement efficace du projet ; ce n’est pas une réflexion après coup. Un bon contrôle de conception Un système de documentation, tel que « l'acte de naissance » du produit, montre clairement le parcours de conception, du concept au prototype.
Comment planifier le parcours de demande d'enregistrement pendant la phase de prototypage ?
Sur la base du bon travail de préparation de la demande d'inscription , accélérer le développement de dispositifs médicaux peut être assuré, et dans ce processus, chaque élément de données généré doit devenir un support solide pour les futurs documents d'enregistrement. C'est-à-dire que les trois niveaux suivants doivent être systématiquement planifiés :
Définir clairement les exigences concernant les preuves d’enregistrement
La phase de conception du prototype nécessite une analyse approfondie des exigences réglementaires du marché cible. Les principales rubriques qui doivent être vérifiées lors de l'examen des enregistrements, telles que les indicateurs de performance, la biocompatibilité et la sécurité électrique, sont traduites en paramètres techniques spécifiques à vérifier par le prototype. Cela garantirait le développement d’un prototype sur la bonne voie dès le début.
Transformez les données de validation du prototype en preuve d’enregistrement
Le prototype doit subir des tests fonctionnels, de durée de vie et d'utilisabilité conformes aux exigences du système qualité . Tous les tests doivent être effectués selon un protocole standard pré-approuvé, qui doit inclure un enregistrement complet des données brutes et un rapport standardisé. Il s'agira de données hautement contrôlées qui pourront ensuite être directement soumises comme preuves de base pour une future validation de conception, évitant ainsi des tests répétés.
Établir un système transparent pour la documentation de l'historique de conception
Il doit fournir un enregistrement complet du processus allant de la conception à la révision, aux modifications et au résultat. Ce système de documentation naturellement formé dans le processus de contrôle de la conception peut s'avérer être la meilleure preuve pour prouver aux agences de réglementation que le processus de conception est rigoureux et contrôlé, ce qui peut considérablement améliorer l'efficacité et le taux de réussite des examens d'enregistrement.
En d'autres termes, planifier demande d'inscription l'intégration dès la phase de prototype est le meilleur levier pour accélérer le développement de dispositifs médicaux , dans la mesure où elle réduit considérablement les coûts élevés et les retards encourus dans les phases ultérieures du projet en raison des données d'enregistrement supplémentaires, tout en améliorant la standardisation et le taux de réussite de l'ensemble du processus de R&D dès le début, posant ainsi une base solide pour un lancement rapide et stable des produits sur le marché
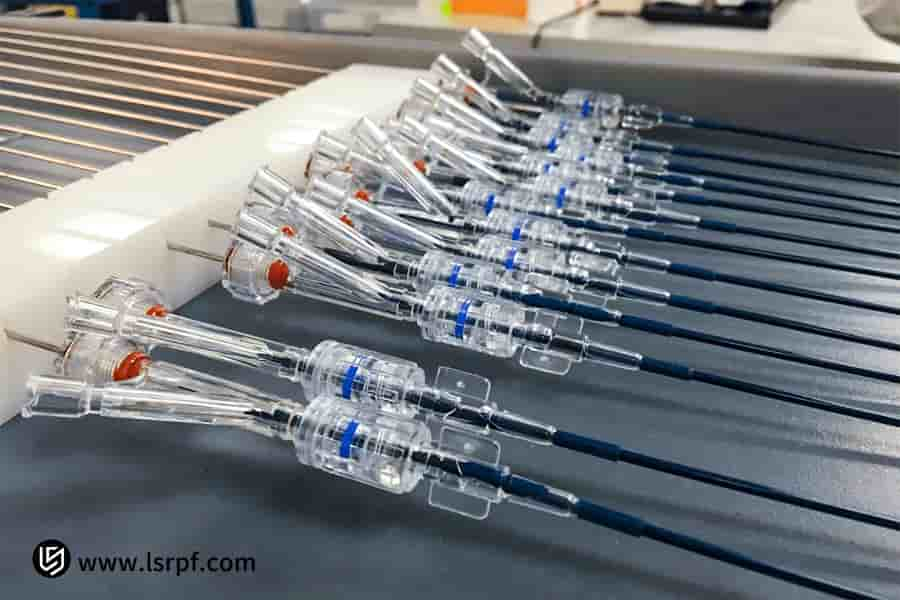
Figure 5 : Prototype à 360 degrés pour validation fonctionnelle par LS Manufacturing
FAQ
1. Quelles exigences spécifiques doivent être respectées lors du développement de prototypes médicaux ?
En outre, au-delà des fonctionnalités de base, il faut veiller de manière proactive au respect des normes particulières relatives aux dispositifs médicaux. Nous appliquons rigoureusement les système qualité ISO 13485 pour s'assurer que ces prototypes répondent aux exigences réglementaires en matière de biocompatibilité, de tolérance de stérilisation, de sécurité électrique et d'autres aspects dès le début de leur enregistrement.
2. Combien de temps faut-il entre la conception et l'obtention du premier prototype fonctionnel ?
Cela dépend de la complexité de l'appareil. Les appareils relativement simples prennent environ 2 à 3 semaines, tandis que les appareils plus complexes dotés de transmissions de précision et de composants électroniques prennent 4 à 6 semaines . Nous disposons d’un canal accéléré pour répondre de manière flexible aux besoins urgents de R&D et garantir pleinement le calendrier de votre projet.
3. Est-il possible de fabriquer de petits lots de dispositifs pour essais cliniques ?
Bien entendu, l'un de nos différents services concerne la fabrication de petits lots de dispositifs d'essais cliniques , allant de 10 à 100 unités . La fabrication était par normes de fabrication de dispositifs médicaux , et chaque unité sera fabriquée selon les exigences de performances, de qualité et de cohérence des essais cliniques.
4. Comment assurez-vous la biocompatibilité des matériaux prototypes ?
Nous contrôlons les risques depuis la source grâce à une sélection stricte de matériaux de qualité médicale dotés de certifications faisant autorité telles que ISO 10993 ou USP Classe VI. Des documents complets de certification des matériaux peuvent être fournis avec le prototype, fournissant ainsi des preuves substantielles pour votre évaluation de biocompatibilité.
5. Comment protégez-vous notre propriété intellectuelle pendant le processus de prototypage ?
La sécurité des informations est notre bouée de sauvetage. Chaque projet commence par un accord de confidentialité juridiquement contraignant et, en interne, nous appliquons un système strict de gestion de la hiérarchie des données et de contrôle d'accès. À la demande du client, des pare-feu physiques et informatiques peuvent également être établis.
6. Quels types de prototypes de dispositifs médicaux soutenez-vous ?
Les services proposés par notre société vont des dispositifs actifs, tels que les équipements de diagnostic, aux dispositifs passifs, notamment les instruments chirurgicaux, les implants et les dispositifs non implantables . Fabrication LS connaît bien les réglementations et les processus associés à divers produits.
7. Comment rendre les données du prototype disponibles pour une utilisation dans les demandes d'enregistrement ultérieur ?
Outre les prototypes, nous fournissons un ensemble complet de preuves de qualité, qui comprend des dossiers de production détaillés, des rapports d'inspection de processus et des données de tests de performances . Tous sont générés selon les spécifications et peuvent être directement utilisés comme matériel de vérification de la conception pour prendre en charge les demandes d’enregistrement.
8. Comment démarrer un projet de prototype de dispositif médical ?
Le processus de démarrage est assez simple : il suffit de remplir quelques esquisses de concept ou exigences techniques initiales, et nous veillerons à ce qu'un ingénieur senior vous contacte dans un délai d'un jour ouvrable pour discuter en profondeur des solutions techniques et vous fournir une première évaluation du projet et un devis.
Résumé
Les prototypes de dispositifs médicaux sont bien plus qu’une réalisation technique ; ils constituent la pierre angulaire de la gestion des risques, de la conformité réglementaire et du succès commercial. Trouver le bon partenaire de prototypage constitue une base solide pour l’ensemble du cycle de vie du produit.
Par conséquent, si vous souhaitez accélérer la R&D tout en réduisant les risques d'enregistrement, veuillez contactez nos experts dans les dispositifs médicaux aujourd'hui pour une « solution de prototypage orientée enregistrement » pour votre projet ! Laissez-nous appliquer notre expérience professionnelle dans la fabrication de dispositifs médicaux pour protéger votre parcours d’innovation.
📞Téléphone : +86 185 6675 9667
📧E-mail : info@longshengmfg.com
🌐Site Internet : https://lsrpf.com/
Clause de non-responsabilité
Le contenu de cette page est uniquement à des fins d'information. LS Manufacturing ne fait aucune déclaration ou garantie, expresse ou implicite, concernant l'exactitude, l'exhaustivité ou la validité des informations. Il ne faut pas en déduire que des fournisseurs ou des fabricants tiers fourniront des paramètres de performance, des tolérances géométriques, des caractéristiques de conception spécifiques, la qualité et le type de matériaux ou des processus via le réseau LS Manufacturing. L'acheteur est seul responsable de ces informations. Pour les devis de pièces, veuillez préciser les exigences exactes de ces pièces. Veuillez nous contacter pour plus d'informations .
Équipe de fabrication LS
LS Manufacturing est une entreprise leader du secteur spécialisée dans les solutions de fabrication personnalisées. Avec plus de 20 ans d'expérience au service de plus de 5 000 clients, nous nous concentrons sur la haute précision Usinage CNC , fabrication de tôle , impression 3D , moulage par injection , estampage des métaux , et d'autres services de fabrication à guichet unique.
Notre usine dispose de plus de 100 centres d'usinage à cinq axes de pointe et est certifiée ISO 9001 : 2015. Nous fournissons des solutions de fabrication rapides, efficaces et de haute qualité à des clients dans plus de 150 pays et régions du monde. Qu'il s'agisse d'une production en petites séries ou d'une personnalisation en masse, nous pouvons répondre à vos besoins dans les 24 heures. Choisir LS Manufacturing, c’est choisir l’efficacité, la qualité et le professionnalisme.
Pour plus d’informations, veuillez visiter notre site Web : www.lsrpf.com .