医疗设备原型确保合规性的核心使命与一般工程原型有着根本的不同。实际上,这就是对慢迭代的误解的根本原因。传统模式中,功能验证与监管验证分离;因此,当面临生物相容性和电气安全等监管挑战时,随后必须对原型进行大幅修改,从而大大延迟了临床试验和注册。
LS Manufacturing 的“以注册为导向的原型设计”策略从设计阶段就以系统的方式嵌入了监管要求。它将标准放在首要位置,确保注册关键要素的满足和原型机功能实现的结合,使原型机具备临床验证和注册测试的资格,从而确保产品上市的一次成功。为了节省您的时间,以下是主要调查结果的简要概述。
医疗设备原型快速参考
| 模块 | 要点 |
| 核心理念 | 创建将功能与法规遵从性结合起来的“注册导向原型”。 |
| 传统痛点 | 在流程后期引入监管要求会导致原型反复修改,从而延迟上市时间。 |
| 关键要素 | 生物相容性、可用性工程和风险管理将在原型设计阶段一起解决。 |
| 解决方案 | 通过积极的监管监督和并行工作,一次性实现正确的设计。 |
| 终极价值 | 大幅降低注册风险,大幅缩短产品上市总周期。 |
下表说明了如何加快医疗器械研发通过改变监管要求 从“后期关卡”到“前期设计投入”。 “以注册为导向”的做法意味着原型本身将成为注册的基础,以后无需进行破坏性修改,以实现高效、可靠、快速的市场投放。
为什么相信本指南? LS制造专家的实践经验
网上有数千篇关于医疗设备原型设计主题的文章,那么您为什么要花时间阅读这篇文章呢?我们在这里分享的不是来自教科书的定义,而是一些受ISO 13485 和 ISO 13485严格约束的实用指南。 ISO9001系统并通过无数的手术和测试结果进行验证。
十多年来,我们的团队制造了超过50,000 个定制原型,满足医疗器械 ISO 13485质量体系要求。每个项目都让我们更深入地了解了如何在不产生热损伤的情况下设置可生物降解镁合金的切削参数,如何在微铣削过程中保持薄壁结构的稳定性,以及如何在迭代的每一步中同时落实风险管理和可用性工程的要求。
相信我们,您在这里读到的是我们每天用来克服挑战的核心方法。让我们共同努力,将您的新颖创意高效、可靠地转化为值得信赖的产品。

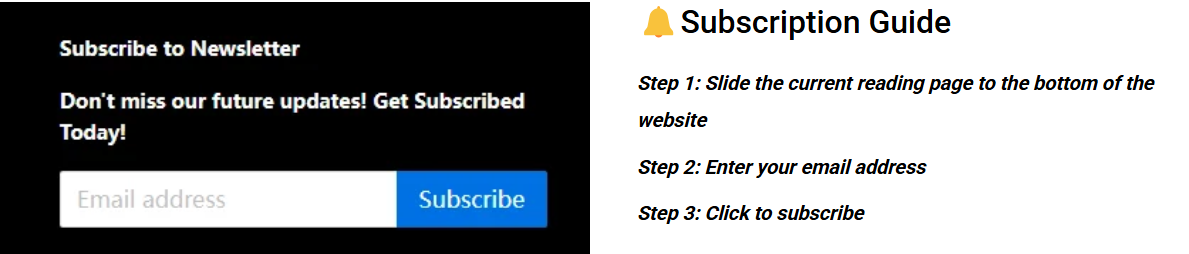
图 1:LS Manufacturing 用于功能验证的综合原型
为什么医疗设备原型应该超越“功能验证”?
医疗器械原型的最终目标不仅仅是成为“工作”模型,而是成为能够通过所有严格的注册和审批流程并安全应用于人体的“产品原型”。因此,其验证范围必须包括使用风险的完整生命周期。
- 无菌耐受性:原型可能具有完美的运动功能,但可能无法承受重复的灭菌过程,例如高温高压、辐射或化学浸泡。材料老化可能会降低其性能并导致临床感染。必须在原型阶段选择和验证合规材料。
- 生物相容性概述:与患者直接或间接接触的部件必须由无毒、不过敏的材料制成。在设计过程后期用生物相容性材料替代可能会影响其机械性能,并需要进行全面的结构重新设计。
- 安全和EMC(电磁兼容性):对于有源器件,样机应提前考虑电气绝缘、漏电流等安全指标,避免运行时影响其他设备而不受外界干扰。后期整改的代价是天文数字,这是注册和测试必须面对的。
嵌入要求监管合规性投入医疗器械原型开发实际上是一种主动的风险管理方法。这将避免由于注册和测试或临床验证过程中出现的功能问题而导致重大设计变更,从根本上节省大量时间和金钱,并成为加快产品上市的基石。
ISO 13485 认证如何影响原型开发的质量体系?
ISO 13485 原型将流程从潜在的偶然活动提升为受控、可追溯且至关重要的流程,从而让人们尽早对最终产品的安全性和有效性充满信心。它要求从概念阶段开始就建立健全的质量体系。这具体体现在:
严格的设计控制和文档管理
对于原型制作,需要根据 ISO 13485 标准提供设计输入、输出、审核和变更的文档。需要完整记录的规格,从客户要求规格到图纸修订记录以及设计审查结论。这也提供了原型与设计意图的一致性,并形成有用的“设计历史”,为后续注册申请提供直接证据。
受控制造和可追溯性
该标准要求对关键原型制作过程进行验证和控制。例如涉及医用级材料,需提供供应商资质证明和进货检验记录;它还涉及加工设备参数的设置和确认,例如层厚度和激光功率3D打印。这将确保 原型设计过程中的一致性和可重复性,为未来的复制或迭代提供了明确的基础。
风险管理的早期整合
风险管理活动应在原型制作期间尽早开始,以识别与应实施控制措施的设计、材料和流程相关的潜在风险。在这方面,它迫使团队提前考虑与安全相关的要求,例如清洁和灭菌以及生物相容性,将解决方案集成到原型的设计和制造中,从而减少以后进行重大设计变更的可能性。
该值来自于质量体系贯穿整个原型制作过程的过程远远超出了获得ISO 13485证书的范围。这将为原型本身产生一个标准化和透明的框架;不仅是一个功能性的“样品”,而且是一个可靠、数据完整、风险可控的“预产品”。
选择符合生物相容性要求的医用级材料?
选择是医疗器械原型开发中确定产品的生物相容性和安全性的第一道关卡。选择合适的材料可以最大限度地降低注册风险,但最重要的是确保患者安全。为了明确选择逻辑,下面对关键考虑因素进行比较。
| 考虑因素 | 基本路径:认证材料的选择 |
高级路径:材料的生物学评价 |
| 原则 | 使用医疗级材料先有成熟的认证,例如USP Class VI 或 ISO 10993。 | 如果使用创新材料,则需要根据ISO 10993 标准进行完整的生物学评估。 |
|
适用场景 |
适用于大多数成熟、低风险、路线清晰、快捷的材料。 | 适用于风险和成本较高的新型创新材料或全新的人与人交互场景。 |
| 关键证据 | 材料供应商填写完整的认证证书和测试报告。 |
委托配备适当且合格的实验室来执行全部或部分所需的安全测试。 |
| 我们的支持 | 我们根据经过验证的医用级材料数据库提供快速匹配和建议,以及评估方案和测试支持的咨询。 | 我们支持客户在整个流程中降低合规风险。 |
我们强烈建议从原型设计的早期阶段就开始规划生物相容性,从经过验证的数据库中选择预先认证的材料,以最大程度地减少不确定性。如果要满足创新需求,则需要提前规划完整的生物学评估路径。这将从一开始就避免因重大问题而导致注册延迟和设计中断,为产品的安全和快速上市奠定基础。

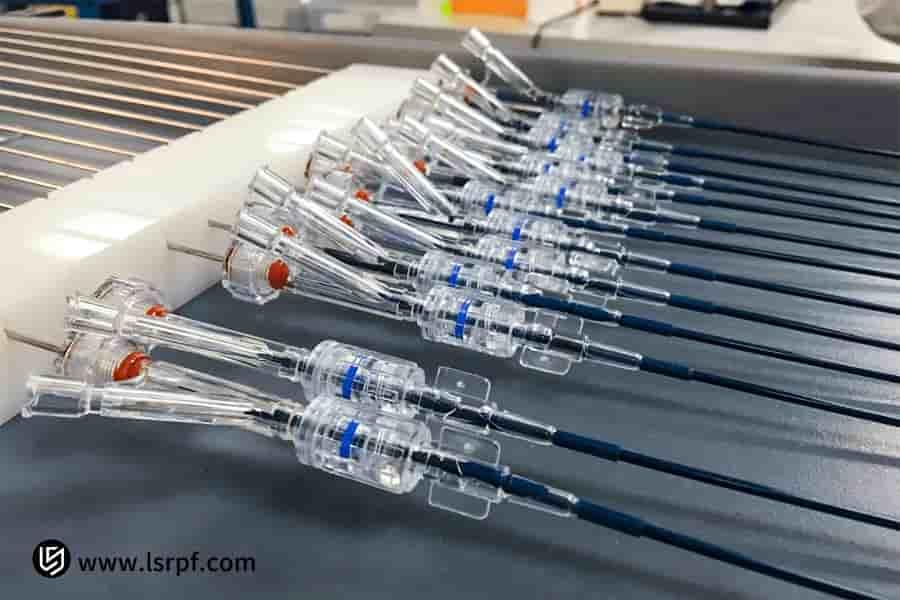
图 2:LS Manufacturing 对医疗原型的精确体积控制
不同临床阶段的原型应该满足哪些标准?
大多数人都误解了医疗设备原型设计作为一项活动,其中原型的一个版本试图满足所有需求。这往往会导致使用中的资源浪费或缺乏标准。从概念到临床验证的每一步,科学精确支持的是根据不同临床阶段的目标制作“恰到好处”的原型。
| 临床阶段 | 原型核心目标 | 生产标准和策略 |
| 概念证明 | 尽快验证设计理念的可行性。 | 经济、快速的方法,如3D打印,可以实现核心功能。材料是无限的;现在是快速迭代的时候了。 |
| 功能测试 |
对原型进行全面的工程测试。 |
使用接近代表产品尺寸、材料和性能的原型对产品性能和可靠性进行彻底验证。 |
| 动物测试 | 该程序的第一步是评估相关产品的安全性及其生物相容性。 | 它必须由生物相容性医用级材料在无菌处理后制备,以便测试有效。 |
| 临床验证 | 安全性和有效性数据应在人体试验中获得。 | 原型必须能够代表最终产品并应符合医疗器械规范涉及性能、材料和制造工艺。 |
一般来说,医疗设备原型设计采用动态但渐进的方法有效地工作。从“经济型”概念验证阶段到“准商业化”阶段, 临床验证原型设计的每个阶段都应该设定一定的目标和相匹配的标准。这样的策略将有效控制早期研发成本,同时确保原型数据链的完整性和可靠性,从而避免因原型标准不匹配而导致项目延误或失败。
手术器械原型如何平衡精度和可制造性?
在这个过程中手术器械原型开发的目的不仅是为了实现更好的功能精度,也是为了证明其设计可以稳定、经济地转化为量产的合格产品。应优先考虑可制造性设计原则。因此,必须考虑以下几点:
结构简化和装配优化
在保证功能的同时,应尽量减少零件数量,避免内部结构复杂。例如,可以使用集成3D打印技术代替传统的多部件组装结构,或者可以采用自锁卡扣设计代替螺钉紧固。这样做,可以大大降低后期的组装难度和时间,从而提高生产效率和一致性。
匹配制造工艺和公差设计
在原型制作阶段,应考虑批量生产所涉及的工艺,例如精密注塑成型和5轴加工,并应设定合理的公差。如果配合尺寸不严格,则不必追求极高的精度;否则,加工成本将急剧增加。设计人员需要了解不同工艺的能力边界,在满足临床要求的同时为制造误差留出合理的余量。
材料及表面处理量产的可行性
原型机的材料选择不仅要满足生物相容性和机械性能的要求,还要考虑供应链的稳定性和批量生产的成本。同时,特殊的表面处理,例如抗菌涂层,应该能够在批量零件而不是实验室样品上稳定且均匀地实施。
成功的手术器械原型从一开始就考虑了可制造性。它可以识别并优化大规模生产中可能出现的制造、质量和成本问题。这个想法是为了避免设计出无法生产或制造成本过高的“完美”产品,并确保从原型到大规模生产的顺利过渡。
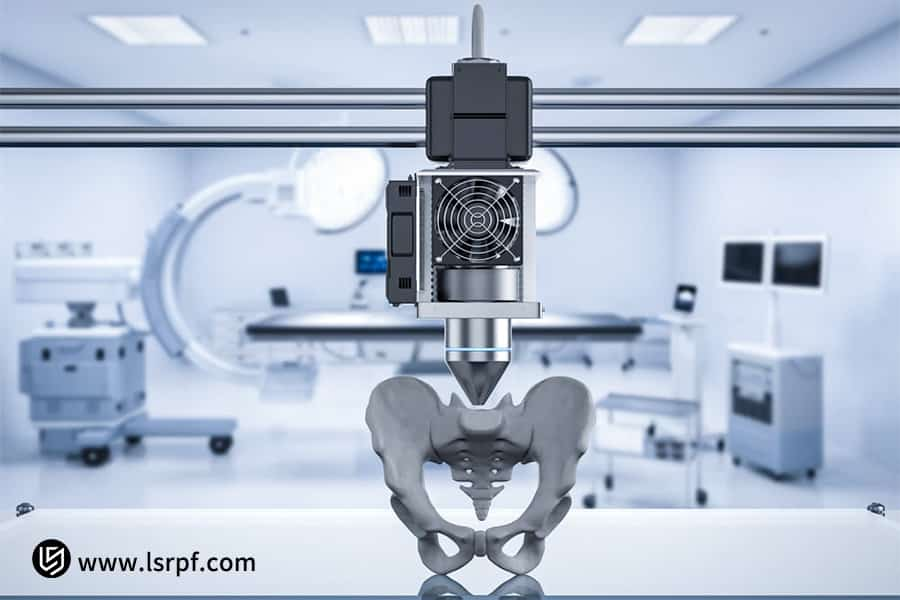
图 3:LS Manufacturing 加速开发定制手术植入物
快速原型技术如何促进医疗器械创新?
最重要的价值医疗设备快速原型制作最大的优点是可以缩短从概念设计到物理验证的时间周期,为试错和迭代提供非常有效的平台。其中,医疗级3D打印正在发挥着革命性的作用,其优势和要求具体体现在:
- 实现复杂结构和个性化定制:传统方法难以加工的复杂微通道和多孔骨小梁结构,可以通过医疗级3D打印轻松生产。因此,可以制造出完全符合患者解剖结构的个性化手术导板和植入物,这一发展直接有助于精准医疗。
- 多种材料和功能的整合:这些现代快速原型技术使组件能够由一系列从刚性、柔性到可生物降解的材料制造,所有这些都在一个组件内。例如,可以一步打印出将刚性框架与软密封件相结合的集成组件,以用于模拟真实器官的解剖模型或复杂药物输送装置的原型。
- 满足医疗应用的特殊要求:无论速度有多快,在医疗设备的快速原型设计中都不能牺牲安全性和合规性。材料必须具有生物相容性,并且打印过程本身必须经过验证,以确保根据质量体系要求确保批次之间的一致性以及整个过程的可追溯性。
这些是一类快速原型技术,其中医疗级3D打印使研发团队能够以更低的成本和创纪录的时间探索以前不可能的设计。对材料和工艺的严格控制确保创新从初始阶段到临床验证和产品注册都遵循合规轨道。
LS Manufacturing如何帮助微创手术器械突破技术瓶颈?
我们提供的创新医疗器械研发的核心价值与其医疗器械原型设计服务帮助客户克服推出产品的关键技术瓶颈。时间下面是一个典型的案例说明,展示了该方法的应用LS Manufacturing 医疗原型方法:
客户挑战
一家创新公司在开发一种新型微创手术器械——腔内吻合器的过程中,在动物试验中遇到了巨大的障碍。核心传动机构在操作中表现出明显的滞后性,无法为外科医生提供对吻合动作的有效和精确的控制。受传统制造工艺的限制,其内部传动结构复杂,已无进一步优化的空间。
LS制造解决方案
经过干预,我们的工程团队立即放弃了传统的加工方法。我们雇用了医用级不锈钢3D打印技术,制造具有优越机械路径和极小间隙的一步式、一体式传动系统。这不仅解决了滞后问题;进一步的改进是对这个复杂的一体成型腔体进行了电解抛光,使其表面光洁度远远超过标准,完美满足手术工具无菌和清洁的极高要求。
结果和价值
在随后的动物试验中,新制造的样机运行完美,仪器的操作响应速度和准确性提高了约60% ,赢得了临床专家的高度评价。这一技术突破直接将客户的整体项目工期提前了至少5个月,并节省了超过200万元的反复试错和模具修改的研发成本。
我们应用医疗级 3D 打印等先进技术来克服常见结构、材料和性能限制微创手术器械为我们的客户。听起来不可能的技术挑战变成了关键的产品竞争力,为我们的客户确保了宝贵的上市时间和巨大的成本优势。

图 4:LS Manufacturing 医疗原型制造中的精确剂量
医疗器械原型开发需要什么类型的技术文档?
满的技术文档是医疗器械注册成功的基石。它主要用于全面记录设计控制过程,并为产品的安全性和有效性提供证据。这不仅可以作为内部发展的路线图,也可以向监管机构证明企业系统化、合规化的发展能力。包括但不限于以下关键文件:
- 设计输入和输出文件:这是文件系统的开始:设计输入,应清晰地记录用户需求、临床功能、性能指标和监管标准。设计输出将包括产品图纸、技术规格、零件清单等。每个输入都应该经过验证才能有相应的输出。
- 材料认证和生物相容性文件:应提供所有医疗级材料的供应商认证和材料证书,以及与 USP VI 级或 ISO 10993 部分相关的生物相容性评估或测试报告。这直接关系到产品的生物相容性的建立。
- 制造过程验证记录:证明原型制造过程对于其创建过程中涉及的每个关键过程来说是一致且可控的,例如3D打印参数或灭菌过程,通过详细的过程参数记录、设备校准证书和首件检验报告。
换句话说,这意味着将技术文档的创建作为与原型制作并行的基本活动,为高效的项目进展做好准备;这不是事后的想法。一个好的设计控制文档系统,例如产品的“出生证明”,清晰地展示了从概念到原型的设计轨迹。
原型阶段如何规划注册申请路径?
在做好注册申请准备工作的基础上, 加快医疗器械研发可以放心,在这个过程中,产生的每一条数据,都是为了成为以后注册文件的有力支撑。也就是说,要系统规划以下三个层面:
明确定义有关注册证据的要求
原型设计输入阶段需要深入分析目标市场的监管要求。注册审核时需要检查的主要项目,如性能指标、生物相容性、电气安全性等,都被转化为具体的技术参数,由原型机进行验证。这将确保原型的开发从一开始就走在正确的合规轨道上。
将原型验证数据转化为注册证据
原型应经过符合质量体系要求的功能、寿命和可用性测试。所有测试都必须按照预先批准的标准协议进行,其中应包括完整的原始数据记录和标准化报告。这将是高度受控的数据,然后可以直接提交作为未来设计验证的核心证据,从而避免重复测试。
建立透明的设计历史记录系统
它应该提供从设计输入到审查、更改和输出的整个流程的完整记录。这种在设计控制过程中自然形成的文件系统,可以成为向监管机构证明设计过程严谨、受控的最佳证据,可以大大提高注册审查的效率和成功率。
换句话说,规划注册申请样机阶段的集成是加速医疗器械开发的最佳杠杆,它有力地降低了项目后期因补充注册数据而带来的高昂成本和时间延误,同时从一开始就提高了整个研发过程的标准化和成功率,为产品快速稳定的上市奠定了坚实的基础
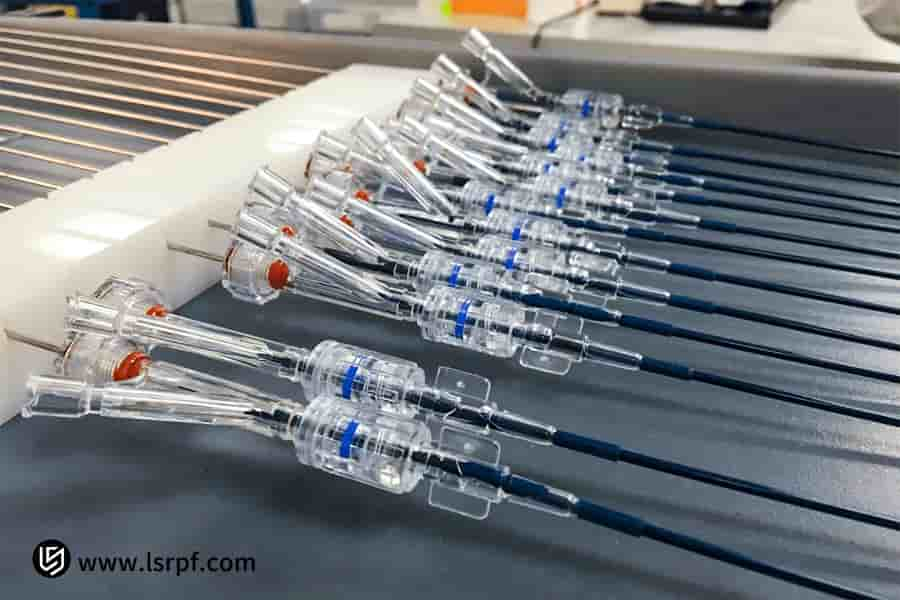
图 5:LS Manufacturing 用于功能验证的 360 度原型
常见问题解答
1. 医疗原型设备的开发过程中必须遵循哪些具体要求?
此外,除了基本功能之外,还需要主动满足医疗设备的特定标准。我们严格应用ISO 13485质量体系确保这些原型在注册之初就满足生物相容性、灭菌耐受性、电气安全和其他方面的监管要求。
2. 从概念到获得第一个功能原型需要多长时间?
这取决于设备的复杂程度。相对简单的设备大约需要2-3 周,而具有精密传动装置和电子元件的更复杂的设备则需要4-6 周。我们拥有加急通道,灵活解决紧急研发需求,充分保障您的项目进度。
3. 是否可以做小批量的临床试验器械?
当然,我们的各种服务之一是小批量临床试验设备制造,数量从10 到 100 台不等。制造是由医疗器械制造标准,每个单元都将按照临床试验所需的性能、质量和一致性进行制造。
4. 如何保证原型材料的生物相容性?
我们通过严格挑选具有ISO 10993或USP Class VI等权威认证的医疗级材料,从源头控制风险。完整的材料认证文件可以与原型一起提供,为您的生物相容性评估提供实质性证据。
5. 在原型制作过程中,你们如何保护我们的知识产权?
信息安全是我们的生命线。每个项目都从具有法律约束力的保密协议开始,在内部,我们应用严格的数据层次管理和访问控制系统。如果客户要求,还可以建立物理和信息防火墙。
6. 你们支持什么类型的医疗设备原型?
我们公司提供的服务范围从有源设备(如诊断设备)到无源设备(包括手术器械、植入物和非植入设备) 。 LS制造熟悉与各种产品相关的法规和流程。
7. 如何让原型数据可供后续注册申请使用?
除了原型之外,我们还提供完整的质量证据包,其中包括详细的生产记录、过程检验报告和性能测试数据。所有内容均按规格生成,可直接用作设计验证材料以支持注册申请。
8. 如何启动医疗器械原型项目?
入门流程非常简单:只需填写一些初步的概念草图或技术要求,我们将确保高级工程师在一个工作日内与您联系,深入讨论技术解决方案,并为您提供初步的项目评估和报价。
概括
医疗设备原型不仅仅是技术实现;它们是风险管理、合规性和商业成功的基石。找到合适的原型制作合作伙伴为整个产品生命周期奠定了良好的基础。
因此,如果您想加快研发速度,同时降低注册风险,请联系我们的专家今天在医疗设备领域为您的项目提供“面向注册的原型解决方案” !让我们运用我们在医疗器械制造方面的专业经验,为您的创新之旅保驾护航。
📞电话:+86 185 6675 9667
📧邮箱:info@longshengmfg.com
🌐网站: https://lsrpf.com/
免责声明
此页面上的内容仅供参考。 LS Manufacturing 对信息的准确性、完整性或有效性不作任何明示或暗示的陈述或保证。不应推断第三方供应商或制造商将通过 LS Manufacturing 网络提供性能参数、几何公差、具体设计特性、材料质量和类型或工艺。买方对此信息承担全部责任。对于零件报价,请注明这些零件的确切要求。请联系我们获取更多信息。
LS制造团队
LS Manufacturing是行业领先的公司专注于定制制造解决方案。拥有20多年服务超过5000家客户的经验,我们专注于高精度数控加工,钣金加工, 3D打印,注塑成型,金属冲压等一站式制造服务。
我们的工厂拥有 100 多台最先进的五轴加工中心,并通过了 ISO 9001:2015 认证。我们为全球150多个国家和地区的客户提供快速、高效、高质量的制造解决方案。无论是小批量生产还是大规模定制,我们都能在24小时内满足您的需求。选择LS Manufacturing,意味着选择效率、品质、专业。
欲了解更多信息,请访问我们的网站: lsrpf.com 。